3-D模型可以揭示致命肺部疾病的新治疗方法
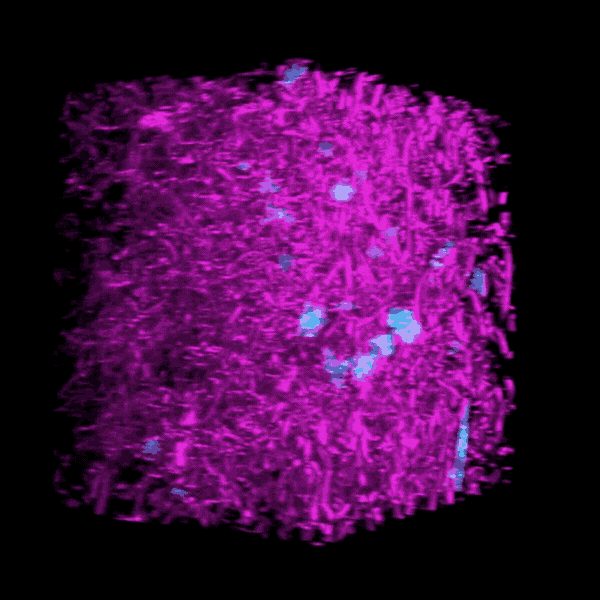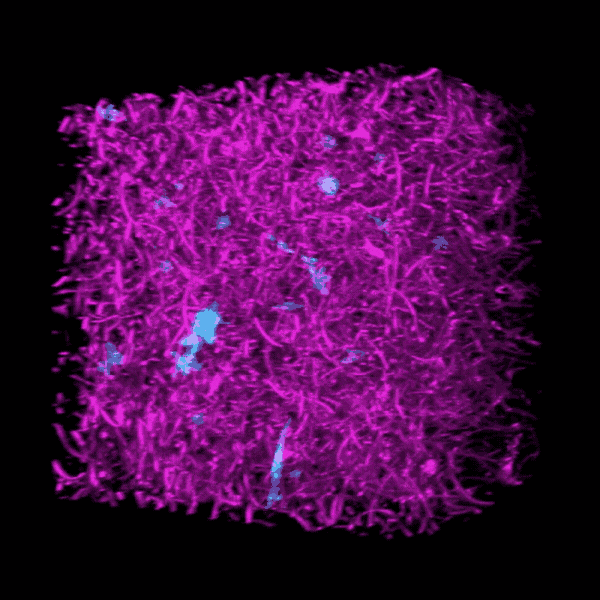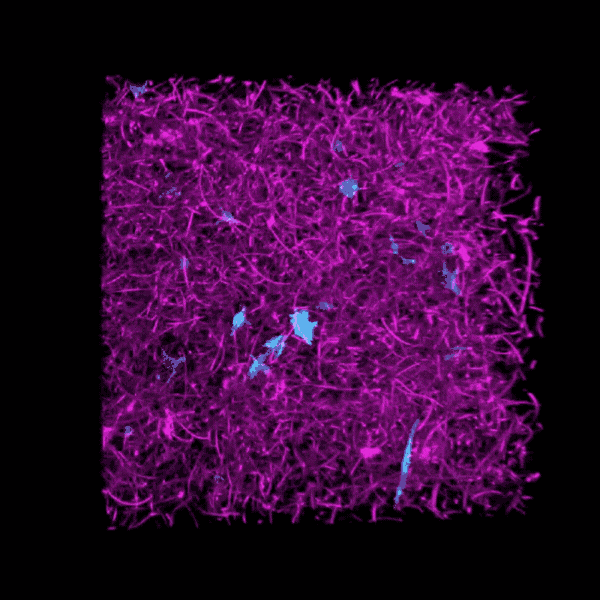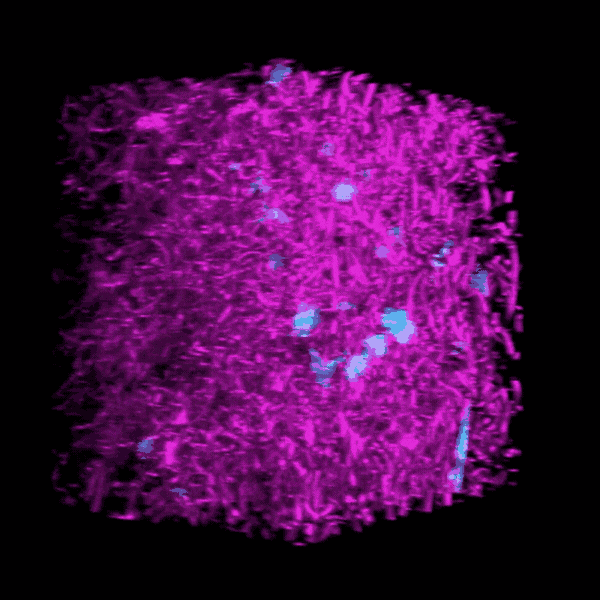
由密歇根大学研究人员建造的三维生物工程模型是几十年来挖洞,培养的培养皿观察致命疾病肺纤维化的进展。
肺纤维化的原因还不完全清楚,但这种情况以疤痕为标志组织在肺部内形成。瘢痕组织使肺部气囊的墙壁变硬,称为肺泡,或在先进阶段,它可以完全填充肺泡空间。这两种情况都使呼吸困难,并降低进入血液的氧气量。通常情况是不可逆转的,最终导致肺部失败和死亡。
一些临床医生担心,重症COVID-19患者在ICU长时间住院后可能会出现某种形式的肺纤维化。
研究人员正在寻找更好的治疗方法。虽然他们设法找到一些缓解症状或在实践中缓慢进展的药物,但他们不能总是在今天的二维实验室模型中复制这些结果。所以他们不明白这些药物如何或为什么如何工作,他们不能总是预测哪些化合物会产生差异。U-M的新研究逐步朝着那方向进行了一步,它披露了现有方法无效的方法。
该团队显示,在一些二维模型中,已知对治疗有效的药物并没有产生显示疗效的测试结果。然而,他们对纤维化肺组织的3d组织工程模型显示,这些药物有效。
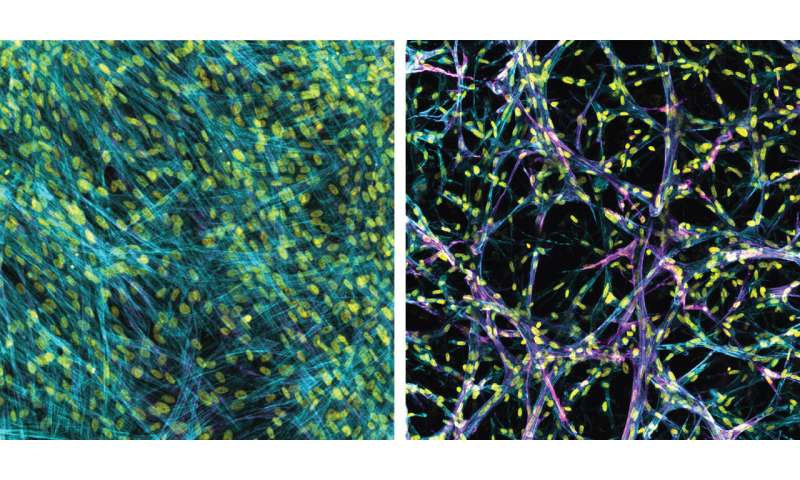
在进行药物测试之前,他们首先进行了研究,以了解组织刚度如何驱动肌成纤维细胞(与瘢痕的发展相关的细胞)的出现。
“即使在来自同一病人的细胞中,我们也看到了不同的结果,”博士生、团队成员丹尼尔·马泰拉(Daniel Matera)说。“当我们将硬度引入二维测试环境时,它激活了肌成纤维细胞,本质上创造了疤痕组织。当我们在3d测试环境中引入同样的硬度时,它阻止或减缓了肌成纤维细胞的激活,停止或减缓了生成疤痕组织”。
随着利用2-D测试的大部分肺纤维化研究,他补充说,许多人认为患者的高肺僵硬是应受治疗的目标。U-M的研究表明,即使它在培养皿中工作,均单独靶向僵硬可能不会阻碍患者的疾病进展。
该小组的研究结果发表在《科学进展》杂志上。
为了找到有效的治疗方法,研究人员首先筛选药物化合物库。如今,他们通常是在扁平的塑料或水凝胶表面培养细胞,但这些设置通常无法重现人体发生的情况。
密歇根大学生物医学工程系的助理教授Brendon Baker和他的团队采用了组织工程的方法。他们重建了三维肺间质(或结缔组织),这是成纤维细胞的所在地,也是纤维化开始的地方。他们的目标是了解来自肺组织的机械线索是如何影响成纤维细胞行为和疾病进展的。
“重新创建肺部插形的3-D纤维结构使我们能够确认在传统筛查环境中不会被确定为命中的有效药物,”Baker表示。
肺纤维化之谜的中心是成纤维细胞,一种在肺间质中发现的细胞,对治愈至关重要,但矛盾的是,它也能推动疾病的进展。当它们被激活时,在受伤后或出现疾病时,它们就会变成肌成纤维细胞。如果调节得当,它们在伤口愈合中发挥着重要作用,但如果调节不当,它们就会引发慢性疾病。在……的情况下肺纤维化,它们引起呼吸呼吸的肺组织的加强。
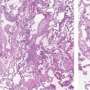
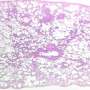
“我们的肺组织模型的外观和行为与我们在真实成像时观察到的相似肺“贝克说”。“我们模型中的患者细胞可以像在疾病中一样积极加强,降低或改造自己的环境。”
本文标题为“微程3-D肺部间质模拟方法突出了肌纤维细胞分化中基质降解的关键作用。”
进一步探索








用户评论