白血病患者midostain药物敏感性的基因组标记物
研究人员已确定急性髓系白血病是一种异质性恶性肿瘤,在NPM1、DNMT3A和FLT3中最常见的基因组改变。Midostaurin是FDA批准的首个用于AML的FLT3抑制剂,是FLT3突变患者诱导化疗的标准治疗方法。由于有一个反应谱,研究人员假设,除了FLT3之外的生物因素可能在药物敏感性中发挥作用,选择FLT3- itd阴性样本也可能表现出敏感性。
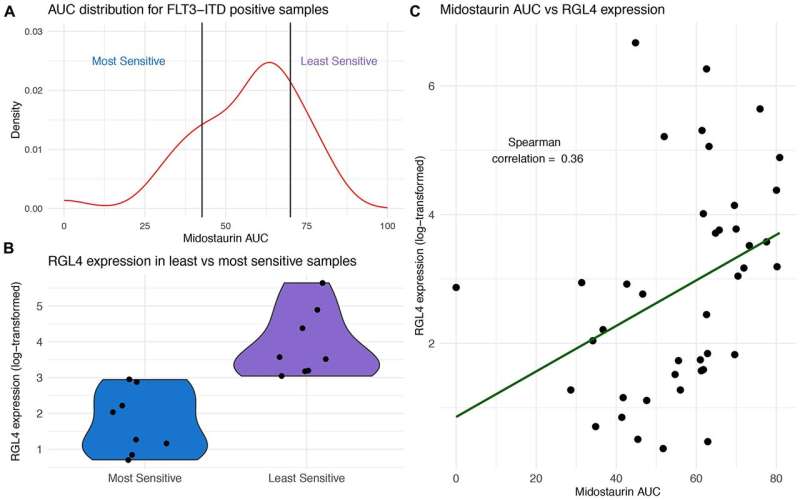
该研究的作者发表在Oncotarget,进行了活体实验药物敏感性对原发性和复发性AML样本进行筛查,并进行相应的靶向测序和RNA测序。他们观察到FLT3-ITD突变与midostain敏感性如预期的相关,并观察到FLT3-ITD阴性样本中KRAS和TP53突变与midostain耐药相关。此外,他们还发现了不受FLT3-ITD状态影响的敏感和耐药样本中差异表达的基因。
在FLT3-ITD突变样本中,RGL4、癌基因和Ras-Raf-MEK-ERK级联调控因子的过表达,区分了耐药和敏感样本。
俄勒冈健康与科学大学的Mara W. Rosenberg博士说:“急性髓系白血病(AML)是一种异质性恶性肿瘤,最常影响≥60岁的个体。”FLT3突变发生在大约30%的新生AML病例中,其中25%为ITD突变,5%为酪氨酸激酶结构域点突变。根据2017年欧洲白血病网络指南,一个完整的诊断工作应该包括筛查FLT3突变的存在,以及突变与野生型等位基因比率。
过去和现在有许多临床试验检测酪氨酸激酶抑制剂对FLT3突变型AML的活性,包括舒尼替尼、米多替林、列司替尼、索拉非尼、ponatinib、crenolanib、吉特替尼和quizartinib。预测耐药性发展的因素包括最初存在多个白血病克隆,低FLT3突变等位基因比率,或FLT3激酶结构域的其他主要突变。
作者推测FLT3-ITD之外还有其他的基因组改变和基因表达变化突变能够影响AML样本耐药或对米多妥林的敏感性,并旨在进一步确定这些因素。
Rosenberg研究小组写道:“我们鉴定了与FLT3-ITD状态无关的中索陶林反应相关的基因组改变,提出Ras-Raf-MEK-ERK抑制联合治疗可能会限制对米多司妥林的耐药性,并提示在AML总体人群中,对于某些表达谱的患者,米多司妥林可能有治疗益处。”











用户评论