研究揭示基因治疗后视网膜和视觉功能的恢复
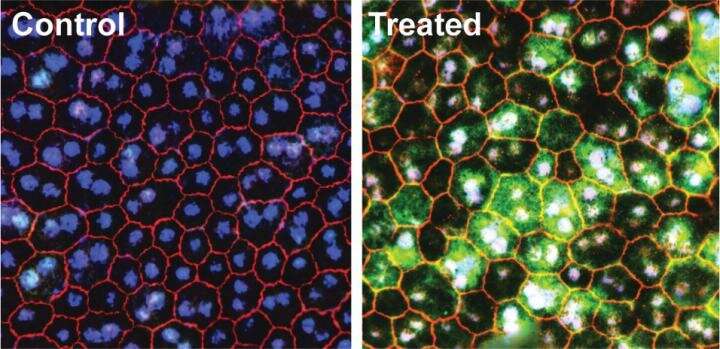
由加州大学欧文分校的研究人员领导的一项突破性研究,使患有遗传性视网膜疾病的小鼠模型的视网膜和视觉功能得以恢复。
今日出版于自然生物医学工程这篇论文的题目是“成年小鼠视觉功能的恢复”视网膜疾病通过腺嘌呤碱基编辑,“说明了新一代CRISPR技术的使用,并为开发一种新的治疗方式,以治疗由不同基因突变引起的各种遗传性眼部疾病奠定了基础。
“在这项概念验证研究中,我们提供了基编辑器在纠正引起遗传性视网膜疾病的突变和恢复视觉功能方面的临床潜力的证据,”Krzysztof Palczewski博士说,他是欧文·h·利奥波德(Irving H. Leopold)主席,也是加州大学医学院眼科加文·赫伯特眼科研究所的杰出教授。“我们的研究结果证明了迄今为止使用基因组编辑最成功地拯救了失明。”
遗传性视网膜疾病(IRDs)是由250多种不同基因突变引起的一组致盲疾病基因.在此之前,没有任何方法可以治疗这些毁灭性的致盲疾病。最近,FDA批准了第一个基因增强疗法,用于治疗Leber先天性黑朦(LCA),这是一种常见的IRD,起源于儿童时期。
“作为基因增强疗法的替代方案,我们应用了新一代CRISPR技术,被称为‘碱基编辑’,作为遗传性视网膜疾病的治疗方法,”UCI医学院眼科助理专家、第一作者Susie Suh说。
“我们通过利用胞嘧啶和腺嘌呤碱基编辑器(CBE和ABE)克服了CRISPR-Cas9系统的一些障碍,例如不可预测的脱靶突变和低编辑效率。使用这些编辑器使我们能够以精确和可预测的方式纠正点突变,同时最大限度地减少可能导致不良副作用的意外突变,”联合第一作者Elliot Choi说,他也是UCI眼科的助理专家。
使用LCA小鼠模型,在临床相关的致病性突变Rpe65UCI团队成功地证明了碱基编辑在治疗LCA和扩展其他遗传性致盲疾病方面的治疗潜力。在其他结果中,碱基编辑治疗使LCA小鼠的视网膜和视觉功能恢复到接近正常水平。
帕尔切夫斯基说:“在接受治疗后,我们研究中的小鼠可以从方向、大小、对比度和时空频率等方面区分视觉变化。”“这些结果非常令人鼓舞,代表着遗传性视网膜疾病治疗的重大进展。”
鉴于眼睛的可及性、其免疫特权地位和成功的临床试验,治疗遗传性视网膜疾病的基因治疗方法具有特别的意义RPE65基因增强疗法导致了第一个美国食品和药物管理局批准的基因疗法。现在,正如本研究所证明的那样,碱基编辑技术可以提供另一种基因增强治疗的治疗模式,以永久地挽救因失明而丧失的关键视觉相关蛋白的功能突变.
进一步探索











用户评论