亚细胞流量的变化增加放射性癌细胞的侵袭性
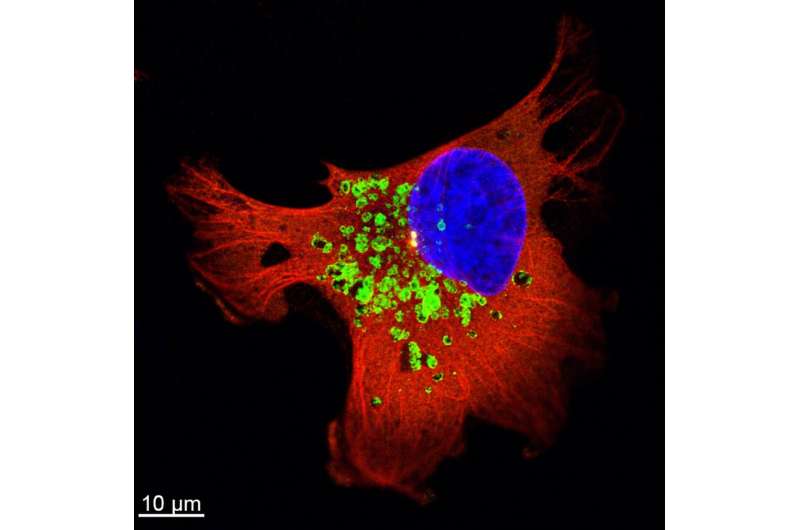
科学家揭示了调节溶酶体运输的分子机制,从而增加放射治疗后耐药癌细胞的侵袭性。
放射疗法是一种有效且常用的治疗方法癌症。然而,有品种癌症对这些疗法产生抗性,并且在某些情况下,这些放射性癌癌症可能会在治疗后变得更加侵入性,恶化患者的预后。
来自日本北海道大学和美国斯坦福大学合作的全球生物医学科学与工程中心的科学家揭示了这一机制分子ar18b和BORC可导致放疗后耐药癌细胞的侵袭和转移。他们的研究结果发表在该杂志上通信生物学。
以前的工作表明,贩运细胞内的囊泡在癌细胞侵袭中发挥着重要作用。一种称为溶酶体的囊泡是特别显着的。溶酶体作为负责分子降解的囊泡而闻名,但它们也参与了用于细胞粘附,肿瘤侵袭和转移的分子的分泌。在目前的工作中,科学家们调查了对放射乳腺癌中这些作用的分子基础。
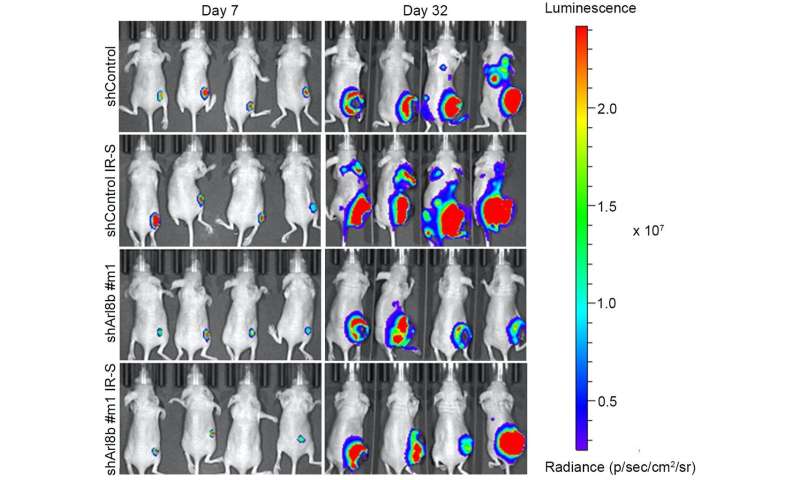
他们首先证实了放射治疗后,溶酶体在癌细胞中的转运上调,增强了降解癌细胞周围结缔组织的酶的分泌,从而增加了癌细胞的侵袭性。他们进一步研究了这种活性背后的分子机制,确定了调节分子Arl8b是这一过程的主要负责人。
ar18b的活性形式通常负责细胞内溶酶体的运输。科学家们观察到,在放射性耐药的癌细胞中,放射治疗后ar18b的活性形式增加,使其能够与其他分子相互作用从而增强溶酶体贩运。此外,通过击倒ARL8B,科学家们表明,该分子是侵袭性和转移的增加。
研究人员分析了数据乳腺癌患者从癌症基因组图谱(TCGA)中识别可能参与其中的其他分子。他们发现,除了ar18b水平外,预后还与一组名为BORC复合体的蛋白质水平有关,BORC复合体由8个亚基组成。高ar18b水平与预后差;此外,可以基于不同硼管亚基的水平来分层预后。ARL8B和溶酶体的关联需要硼管。科学家们认为某些硼管亚基需要增加胃肠癌的侵袭性细胞由Arl8b;此外,放疗还上调了某些BORC亚基表达的基因。
在这项研究中,科学家们发现放射疗法对溶酶体贩运的影响以及控制该过程的一些分子。澄清了这一点分子基础对于这一机制,必须对来自人类癌症患者的更大数据集进行分析,以验证研究结果。此外,针对这一机制的药物必须开发和评估为癌症疗法。
进一步探索















用户评论