FDA小组审查了20年来首个阿尔茨海默病新药

美国监管机构正在考虑是否批准第一种据称可以减缓阿尔茨海默病(最常见的痴呆症)智力衰退的药物,这是几十年来最大的药物决策之一。
一个外部专家小组周五开会,为美国食品和药物管理局(Food and Drug Administration)提供有关aducanumab的建议药物来自马萨诸塞州剑桥市的Biogen Inc.和日本卫材公司(Eisai Co.)。FDA并不总是听从委员会的建议,但通常会听从,而且要到3月份才能做出决定。
这种药物不能治愈或逆转阿尔茨海默病;这种说法是,它适度地减缓了下降的速度。
证据尚不明确:两家公司去年停止了两项研究,因为这种药物似乎没有效果,然后又改变了态度,说有更多的结果表明,在一项研究中,这种药物在高剂量下是有效的。结果尚未公布。
周三发布的一份FDA工作人员报告给出了普遍乐观的看法,称积极的研究可能“非常有说服力”。但FDA的一名统计学家指出了结果中的缺陷和不一致,以及潜在的安全问题。
消费者组织“公众公民”警告称,这种药物预计将非常昂贵,“可能会使我们的医疗保健系统破产”,同时给患者带来虚假的希望。
美国有超过500万人患有阿尔茨海默氏症,世界范围内还有更多的人患有阿尔茨海默氏症。目前的药物只能暂时缓解症状,最后一种药物是近20年前批准的。
FDA的评估重点是安全性和有效性。但是,包括阿尔茨海默病协会在内的倡导者正在推动将需求作为决定的一部分。
该协会在给FDA的信中写道,“有一种可怕而迫切的需要”来帮助那些受到这种疾病“残酷现实”影响的人。该协会去年从百健和卫材那里获得了45万美元,不到其总收入的1%。
另一些人则表示,对药物的需求与药物是否有效或安全无关。
“这是一个艰难的决定。我认为无论结果如何,它都会引起争议,”阿兹海默氏症药物发现基金会的首席科学官霍华德·菲利特博士说,他同时也是Biogen的顾问。
关于药物
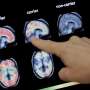
Aducanumab(读作“add-yoo-CAN-yoo-mab”)旨在帮助清除大脑中一种叫做β -淀粉样蛋白的有害团块。其他实验性药物也能做到这一点,但对患者的思考能力、自理能力或独立生活能力没有影响。
这是一种由活细胞制成的生物技术药物,这种药物非常昂贵。目前还没有公布这种药物的估计价格,这种药物每月通过静脉注射一次。Fillit指出,用于其他疾病的Biogen药物每月花费3500美元,加上每次输注的费用。
如果aducanumab获得批准,预计它将被纳入老年医疗保险政府计划。FDA和医疗保险在审查新药或治疗方法时不得考虑成本。
即使获得使用这种药物的资格也可能很昂贵。它只在患有阿尔茨海默氏症的轻度痴呆症或轻度认知障碍的人身上进行了测试。为了验证诊断,需要花费5000美元或更多的脑部扫描。包括医疗保险在内的保险公司不包括扫描,因为它们的好处不清楚,但如果扫描成为治疗的门户,情况可能会改变。
的证据
从历史上看,FDA通常要求两项研究证明安全性和有效性,但近年来放宽了这一标准。
两项aducanumab研究都招募了大约1650人,在药物似乎不起作用时,大约在中途停止。百健说,后来的结果显示,一项研究在最高剂量下呈阳性;第二项研究显然是消极的。该公司表示,对两项研究的分析显示,长时间服用最高剂量的人受益。
但这种分析的有效性存在许多问题。另一个并发症是:研究在进行后改变了,让一些人接受更高的剂量。阳性研究中的安慰剂组比阴性研究中的安慰剂组恶化得更严重,这可以帮助解释为什么aducanumab在那个研究中相比之下表现得更好。
FDA的审查在很大程度上消除了安全性担忧,包括多达三分之一的患者出现脑肿胀,通常导致停药。
梅奥诊所的David Knopman医生说,FDA应该要求在理想条件下测试药物的第三项研究,并得到明确的答案。他在食品药品监督管理局工作顾问小组但他不会投票支持aducanumab因为他帮助领导了一项研究。他和其他医生发表一篇期刊报告本周早些时候反对批准。
这对病人意味着什么
美国国家衰老研究所神经科学主任Eliezer Masliah博士说,这种药物的任何好处“都相对较小”。
在积极的研究中,这种药物适度地减缓了智力衰退的速度——在思维技能得分为18分的情况下,仅相差0.39分。这在独立生活、认识家庭成员或记忆方面有多大意义尚不清楚。
去除淀粉样蛋白的药物可能必须与在大脑中起其他作用的药物联合使用,并在损伤发生之前足够早地使用,才能发挥更大的作用,Masliah说。
如果该药物获得批准,美国神经病学学会敦促FDA不要将其作为广泛的授权,这可能会使许多患者接触到可能有害而不是有益的药物,并可能“压倒医疗保健系统”。
进一步探索
©2020美联社。版权所有。未经允许,本材料不得出版、广播、重写或再分发。