科学家对阿尔茨海默氏症的新治疗目标进行了突破性的发现
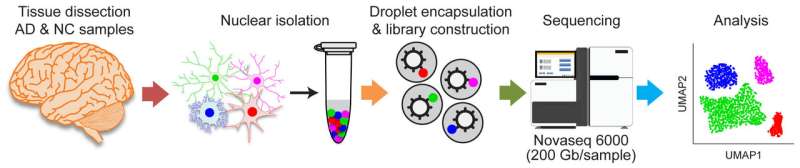
香港科技大学研究人员(HKST)通过使用新开发的方法研究患者的大脑已经确定了阿尔茨海默病(AD)的新治疗目标。这种新方法还使研究人员能够测量潜在药物对广告患者的影响,开启新的广告研究和药物开发的新方向。
虽然已经研究过的广告的病理机制数十年来,但该疾病仍然是可行的。一个原因是传统的研究方法具有有限的能力,识别药物发育的分子目标。分子和病理途径分析通常将AD患者的大脑视为单个单位,这通常低估了不同的贡献脑细胞类型为广告和它们的任何异常。尤其如少常见的细胞类型如小胶质细胞(大脑的常规免疫细胞)和神经血管细胞(特别是内皮细胞),它们分别只占脑细胞总数的不到5%和1%。
但是,由南希知识产权教授领导的团队,分子神经科学国家重点实验室的副主任,HKUST的生命科学教授的主任,不仅仅是污染这个问题 - 他们也发现了几个内皮细胞和微胶质的新潜在分子靶标药物开发。
该团队通过使用先进的单细胞转录组分析,检测了AD患者死后大脑中特定细胞类型的功能,这通常是传统方法不可能实现的,它可以用来表征单细胞的分子变化。这就产生了AD患者大脑转录组中细胞类型特异性变化的全面概况。随后的分析确定了与AD相关的细胞亚型和病理途径,突出了大脑血管中发现的内皮细胞的特定亚群。因此,研究小组发现,增加的血管生成(从现有的血管形成新的血管)和免疫系统激活的亚种群内皮细胞与AD发病机制相关,提示血管失调与AD之间存在联系。研究人员还发现了恢复AD患者神经稳态的新靶点(在外部变化的情况下保持相对稳定的内部状态的能力)。
该团队还利用了它们的单细胞转录组分析来研究细胞因子白细胞介素-33(IL-33),一种免疫信号传导的重要蛋白质的机制施加有益的行为,使其成为可能的广告治疗干预。研究人员发现,IL-33通过刺激微胶质细胞的特定亚型的开发来减少AD样病理,这有助于透明淀粉样蛋白β,一种在AD大脑中发现的神经毒性蛋白质。该团队也是第一个捕获MICROGLIA转化为淀粉样蛋白β-消费吞噬状态的机制的数据,这是除去病原体的主要细胞机制。
叶教授解释说:“大脑内复杂而不同的细胞组成,使得研究疾病机制变得困难。”“单细胞技术的进步使我们能够识别特定的细胞亚型和分子靶点这对于开发新的阿尔茨海默病干预措施至关重要。”
该团队最近在着名的科学期刊上发表了他们的工作国家科学院的诉讼程序U S A(PNA)和细胞报告。
AD,痴呆症的主要形式,目前在全球范围内影响了超过5000万人,并预计将在2050年之前折磨1.5亿人。其病理标志包括细胞外淀粉样蛋白 - β沉积和神经纤维纤维缠结的积累。随着时间的推移,这些病理标志的无效清除导致广告中的细胞功能障碍,导致记忆损失,通信问题,减少身体能力,最终死亡。
刘顺发等。IL-33-PU.1转录组重编程驱动阿尔茨海默病小胶质细胞功能状态转变和清除活性,细胞报告(2020)。DOI:10.1016 / J.CELREP.2020.107530














用户评论