与肥胖慢性炎症有关的血管细胞
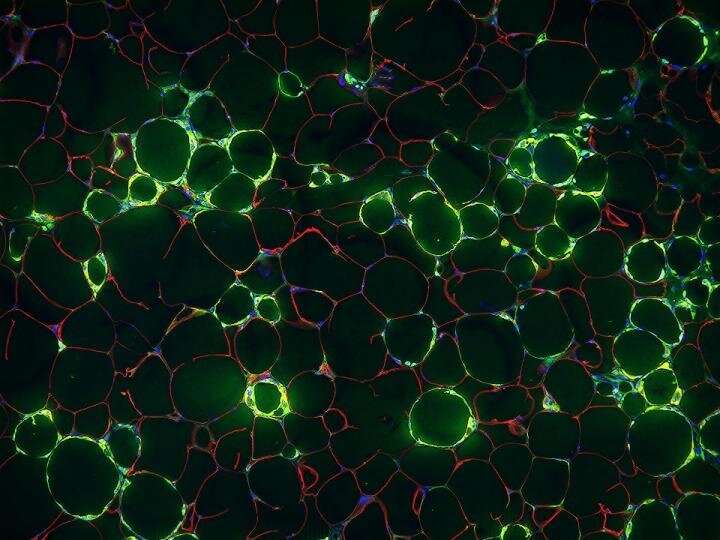
2020年12月30日——当体内的脂肪细胞充满了多余的脂肪时,周围的组织就会发炎。慢性、低水平的炎症是许多与肥胖有关的疾病背后的驱动因素之一。现在,德克萨斯大学西南分校的科学家们发现了一种细胞,至少在老鼠身上是引起脂肪组织炎症的。他们的研究结果发表在自然的新陈代谢可能最终会找到治疗肥胖的新方法。
“脂肪的炎症细胞研究负责人、内科学副教授拉纳·古普塔博士说:“肥胖个体的肥胖与许多我们与超重有关的共病有关——癌症、糖尿病、心脏病和感染。”“通过识别这些细胞,我们在了解导致炎症的一些初始事件方面取得了进展。”
当一个人消耗超过所需的热量时,多余的热量以甘油三酯的形式储存在脂肪组织中,也被称为白色脂肪组织(WAT)。研究人员知道,在肥胖人群中,WAT过度工作,脂肪细胞开始死亡,免疫细胞被激活。但是这种炎症发生的确切机制还不完全清楚。
虽然很多研究都集中在信号分子WAT中的脂肪细胞或免疫细胞可能导致炎症,古普塔的团队采取了不同的方法。相反,他们把注意力集中在了携带血液的血管上免疫细胞和炎症分子——进入WAT。
2018年,Gupta和他的同事们确定了一种新的细胞衬里这些血管在小鼠中 - 脂肪祖细胞(APC)或前体细胞,或前体细胞进行成熟的脂肪细胞。但与大多数APC,新细胞被称为纤维炎祖细胞,或促进炎症的FIPS产生的信号。在新的工作中,研究人员在介导炎症方面的角色仔细观察。
在一天之内将年轻的雄性老鼠换成高脂肪饮食古普塔和他的同事们发现,fip能迅速增加产生的炎症分子的数量。在高脂饮食28天后,他们发现与其他apc相比,FIPs的比例显著增加。
古普塔说:“这是第一次研究表明,这些细胞在脂肪组织中扮演着非常活跃的早期角色,是炎症的守门人。”
为了证明FIPs数量和活性的增加不仅仅是已经发炎的脂肪细胞的副作用,研究小组从一些小鼠的FIPs中移除了一个关键的免疫信号基因Tlr4。在高脂肪饮食5个月后,缺乏Tlr4的小鼠体重和脂肪的增加与其他高脂肪饮食的小鼠一样多。但是基因工程小鼠- FIPs不能再产生相同的信号-不再有高水平的炎症。相反,水平炎性分子它们的WAT水平更接近低脂饮食的老鼠。
Gupta和他的同事继续证明,增加FIPs中相关信号分子ZFP423的水平也可以改善这种疾病炎症在鼠标脂肪细胞。这些发现为降低肥胖人群患病风险提供了可能的途径。
古普塔说:“看起来ZFP423可能是减缓这些细胞炎症信号的重要刹车。”当然,这是否适用于人类还有待观察老鼠。"
古普塔的团队正在计划未来的实验,以更好地了解高脂肪的哪个方面饮食启动FIPs中增加的炎症信号,以及该结果是否适用于人类脂肪。
进一步探索














用户评论