FDA批准经股动脉截肢植入系统

(健康日)——美国食品和药物管理局周五宣布,首个用于经股动脉截肢的植入系统获得批准。
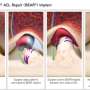
根据2015年的人道主义器械豁免条款,骨锚式假肢(OPRA)植入系统已经上市,适用于不能使用传统假体的膝上截肢成人。OPRA植入系统通过手术进行锚定,并整合到患者的残肢中股骨与传统的假腿不同,传统的假腿是在残肢上安装一个插座,将设备固定在腿上。
植入系统的安装是通过两次手术完成的,间隔6个月。在第一次手术中,外科医生将一个圆柱形的固定物植入其余股骨的中央管中。一旦组织生长固定支架,皮肤愈合后,外科医生进行第二步操作,将附加的设备部件连接到支架上。的植入物该系统通过患者残肢底部的皮肤延伸并与假体连接。第二次手术后,患者必须接受大约6个月的训练和康复,然后才能安装他们定制的假体。
该批准是基于65名接受OPRA植入系统的患者的安全性和有效性数据。经股动脉截肢患者在2年和5年的问卷得分分别比传统的假体患者提高了35.1分和39.6分(满分为100分)。报道的不良事件包括感染、机械并发症、疼痛、损伤和固定装置松动。
OPRA植入系统经过了上市前批准途径的审查,由瑞典Mölndal Integrum AB公司生产。
进一步探索
版权©2020每日健康。保留所有权利。







用户评论