太多的好东西-持续的IFNγ通过BST2耗尽祖血细胞
当一个人被感染时,身体会激活免疫反应来对抗它。IFNγ是免疫系统产生的一种炎症分子,有助于对抗感染。然而,长期暴露于IFNγ有不良后果——它不可逆转地消耗血液干细胞,所有血细胞的祖细胞,包括免疫细胞,通过触发其增殖和过度终末分化。由于缺乏免疫细胞,患者最终无法抵抗感染。
贝勒医学院研究人员研究了IFNγ介导血干衰竭的机制细胞它们通常处于静止状态,这意味着它们处于休眠状态,直到受到刺激时才被激活。他们发表在杂志上细胞的报道IFNγ刺激这些细胞对这些细胞的蛋白质BST2的产生,从而导致它们从静止状态,持续增殖和最终耗尽的出现。结果表明,调节血液干细胞的BST2表达可以提供调节这些细胞激活和/或持续性期间慢性感染的方法。
“我们的研究开始于问,‘当血液干细胞与IFNγ相互作用时发生了什么变化,以及这对它们的繁殖或消耗有什么影响?共同通讯作者凯瑟琳·金博士说,她是儿科传染病学副教授,也是贝勒大学丹·邓肯综合癌症中心的成员。ob体育开户网址
血液干细胞驻留在骨髓中,通常与形成一种巢状细胞的CAR细胞接触。CAR是支持干细胞健康的看护细胞。
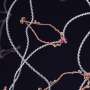
“研究血液干细胞和CAR细胞的实时相互作用活的动物,我们开发了新的小鼠模型,设计在同一动物的血液干细胞(红色)和CAR细胞(绿色)中表达不同的荧光蛋白。该模型使我们能够在活体动物完整的骨骼中分别或同时可视化和跟踪这两种细胞类型,”共同通讯作者Dongsu Park博士说,他是贝勒大学分子和人类遗传学、病理学和免疫学助理教授。
该研究小组将这种方法与先进的活体动物成像技术相结合,发现在正常骨髓中,血液干细胞与CAR细胞之间存在紧密的相互作用,但当暴露于IFNγ时,干细胞出人意料地远离CAR细胞。
King说:“我们认为IFNγ正在破坏干细胞的静止状态,并促进细胞活性。”“我们的下一个实验研究了这是如何发生的。”
研究人员寻找暴露于IFNγ后干细胞表面表达的蛋白质。他们推测IFNγ诱导的表面蛋白可能促进了干细胞与CAR细胞的分离。
“把它想象成干细胞外部的一个粘性标签,它将干细胞带到其他地方。这就是我们如何识别这种名为BST2的蛋白质。”King说。“事实上,在我们敲除BST2的小鼠中,干细胞远离巢的重新定位以及过度增殖和耗尽并没有发生,这支持了BST2在这些功能中的作用。”
归航
研究人员还发现BST2有助于细胞与e -选择素结合,e -选择素是内皮细胞表面的一种蛋白质,比如血管内壁的内皮细胞。这些发现与归巢(homing)有关,归巢是指骨髓移植后的血液干细胞找到返回受体骨髓的途径。
“当我们将干细胞暴露于IFNγ中时,干细胞的归位改善了。我们认为,BST2的增加可能有助于干细胞粘附内皮细胞上的e -选择素,促进细胞通过血血管到达骨髓,”金说。
“BST2是一种令人着迷的蛋白质,人们对它的研究主要是由于它能够保护我们的身体免受病毒感染,以及它在癌症中的作用。最令我兴奋的是,我们是第一个报告BST2在研究中发挥重要作用的小组造血干细胞,它位于顶部免疫系统第一作者Marcus a . Florez说,他是King实验室贝勒医学院医学科学家培训项目(医学博士/博士)的学生。“这个项目对包括慢性感染在内的多种疾病都有重要意义,骨髓失败和移植接受者。”
进一步探索








用户评论