阿片受体MOR1变化发现在神经退行性疾病的模型
亨廷顿氏病是一种致命的遗传疾病,罢工在中年时最常见的情绪障碍,无法控制肢体运动和认知能力下降。年在症状出现之前,大脑成像显示了纹状体的退化,大脑的这一区域主要负责快速选择的行为动作。纹状体神经元退化,他们的“身份”蛋白质,给特定细胞类型的构建块他们独特的功能,逐渐关闭。
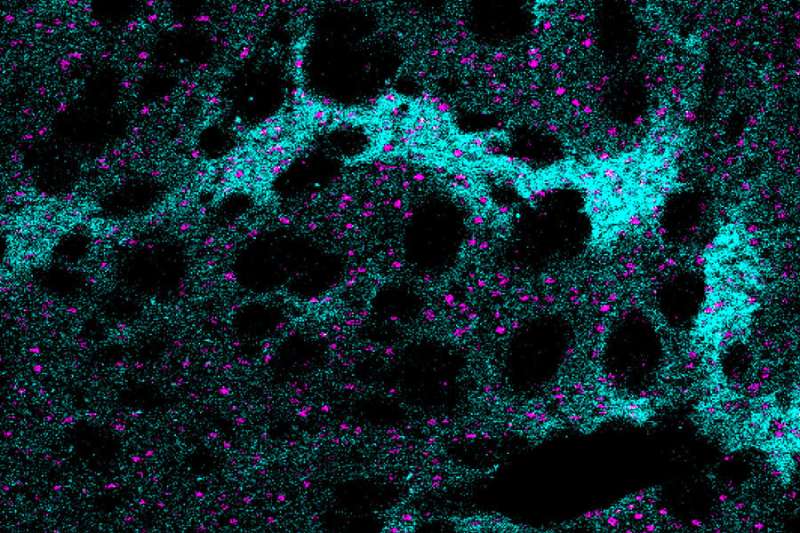
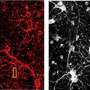
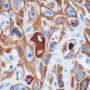
一项新的研究学院教授实验室的安布耶尔发现一个令人惊讶的例外。研究人员发现,在亨廷顿的小鼠模型疾病细胞蛋白质MOR1身份,命名为μ阿片受体类型,实际上变得更丰富的纹状体神经元退化。
“这是其中一个最引人注目的免疫组织化学改变我所看过的文献亨廷顿氏舞蹈症模型动物,“越前Morigaki说,布耶尔实验室的研究科学家和这份报告的主要作者,是曾与Tomoko吉田和其他布耶尔实验室。
更多的阿片受体
MOR1表面受体神经元,结合阿片类药物,是由身体或缓解疼痛,如吗啡。天然阿片类药物在大脑中一个叫做脑啡肽小分子,它通常是由相同的纹状体神经元堕落在亨廷顿氏舞蹈症的早期阶段。
研究小组推测,纹状体增加的数量在亨廷顿氏舞蹈症MOR1受体模型补偿的脑啡肽水平暴跌,但他们也相信这种上调可能扮演一个角色的感觉奖励。
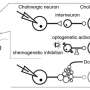
以前的工作表明,MOR1具有明显的信号机制相关函数在药瘾的疼痛知觉和它的功能。这些不同的机制可能与这一事实有关MOR1产生多个亚型,“细微变化的蛋白质,可以读出相同的基因。MOR1异构体的纹状体中发现的被认为是更重要的药瘾行为比疼痛知觉。这反过来意味着MOR1可能发挥作用在纹状体的关键功能,这是学习行为是最有可能导致奖励。
“现在认识到情绪干扰可以早在公开的马达异常杭丁顿氏症患者的许多年。这些甚至可以最令人不安的症状对患者和他们的家庭。阿片类药物的发现,这种受体变得如此高的情绪网站纹状体,至少在小鼠模型的障碍,可能会给一个提示底层电路功能障碍导致这些问题,”布耶尔说。
线索进行治疗
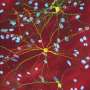
MOR1作为标准来识别子集的神经元位于纹状体神经元簇布耶尔之前发现并命名striosomes。
“最令人兴奋的点对我来说是纹状体的参与隔间(striosomes)在亨廷顿氏病的发病机制,“Morigaki说,他现在已经搬到日本Fukoshima大学,是一个练习神经外科医生对运动障碍。
MOR1-positive striosomal神经元高利息的部分原因是他们有直接连接到相同的多巴胺生成神经元被认为在帕金森病退化。而帕金森病的特点是多巴胺的损失和损失的运动,亨廷顿氏舞蹈症的特点是多巴胺和过度起伏运动。事实上,唯一fda批准的药物来治疗亨廷顿氏舞蹈症是减少多巴胺释放药物,从而努力抑制异常运动。但这些治疗有潜在的严重的副作用,如抑郁症和自杀。
这一最新发现可能提供机械的线索多巴胺亨廷顿氏舞蹈症的波动和提供更具体的治疗途径。
这个故事是由麻省理工学院新闻(再版web.mit.edu/newsoffice/),一个受欢迎的网站,包括麻省理工学院新闻研究、创新和教学。









用户评论