科学家发现一种细胞和分子机制,促进血管动脉血化
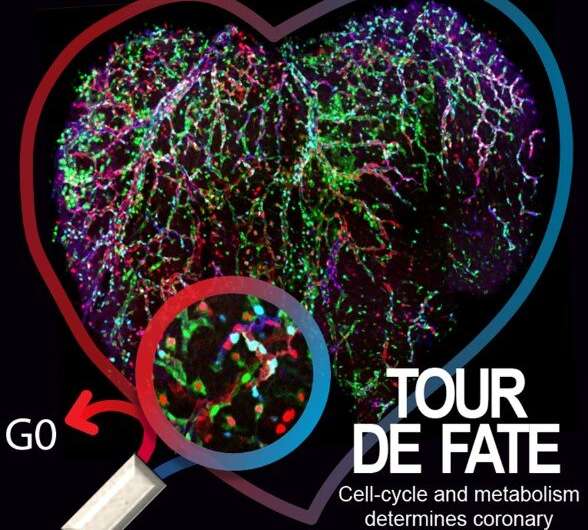
研究由科学家Centro Nacional de Investigaciones心血管为维基百科()提出了对血管生物学的理解,并指出设计新的治疗策略的方式诱导血管化和更有效的受伤或缺血组织的血液灌注。
鲁伊·Benedito领导的研究,并发表在自然,揭示了一个新的发展的至关重要的细胞和分子机制动脉从毛细血管,这一过程被称为动脉血化。激活这个机制可以改善心脏功能的恢复后临时或长期减少心脏的血流量。
直到现在,血管动脉血化被认为依赖祖细胞的分化和规范成一个动脉细胞,这一过程被认为需要转录激活和DNA重建。新发现表明,动脉血化涉及到及时抑制新陈代谢和相反细胞周期,这一事件是两个必要和充分引发的分化和发展的动脉。
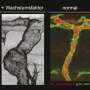
在过去的20年里,科学家已经发现了几个基本的细胞和分子机制形成和分化的动脉和静脉。第一个血管在任何器官是不成熟和发展形成一个未分化的和基本的血管网络称为前体血管丛。这个网络是由内皮细胞和相对低效的运输血液。它可以比作一个道路网络为当地交通但缺乏建造一个更大的系统连接高速公路。
形成一个层次组成更大的传导动脉和静脉血管系统是必不可少的有效的血液与组织运输。“这个系统会导致过早的不正确的发展胚胎死亡或可能致命的疾病有关血管畸形会导致中风,可怜的氧气供应不足或组织灌注,”该研究的作者解释道。
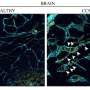
正确的动脉起始规范需要两个基因的激活途径:VEGF和信号通路。“缺口是一个直接调节转录的分子信号通路的一个巨大的数组的基因改变细胞的生物学。切口不激活内皮细胞时,动脉规范和开发失败,剩下的只有毛细血管和静脉内皮细胞,”鲁伊·Benedito说。
这导致了认为动脉通过一个高度保守的感应,Notch-dependent程序的基因改变内皮细胞的一个子集。这种基因程序被认为是必不可少的内皮细胞分化的能力,迁移,形成动脉。
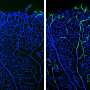
使用复杂的小鼠模型,细胞成像和命运映射工具,鲁伊Benedito集团现在已经发现细胞有明显Notch信号水平偏向特定的命运,而不是预先确定的基因,因为它们可以采用不同的动静脉命运如果放置在适当的生物物理背景。
第一作者温罗发现,VEGF和缺口的主要功能化为动脉血内皮细胞抑制Myc,抑制其促进细胞增殖和代谢的能力。研究表明,Myc抑制是必要的,足以引起一个有效动脉血化的倾向。
结果也有重要意义的使用药物来促进血管生成在缺血性心血管疾病。研究表明pro-angiogenic药物刺激一般血管增殖抑制动脉血化。“我们未来的目标之一是识别新方法可以抑制增殖信号只在pre-arterial细胞,从而促进有效动脉血化没有负面干扰毛细管的诱导血管生成,“鲁伊·Benedito说。
从翻译的角度来看,作者得出结论,能够调节动脉或静脉的身份血血管是极大的兴趣治疗冠状动脉疾病和心肌梗塞。获得的结果可能会导致新的治疗方法诱导有效动脉血化在缺血性心血管疾病。