意外发现揭示了肺癌侵略性形式的新目标
目前有针对性的疗法目前可用于约三分之一的肺腺癌,最常见的肺癌。这些药物通过横截突然促使它们在很大程度上施加健康组织而产生的分子变化来抑制癌细胞。但对于其他三分之二的人进行这种癌症,治疗方案较少。
斯隆·凯特林纪念中心的一个研究小组报告了一种特别具有侵袭性的肺腺癌的新发现,这种癌是由KEAP1和STK11基因中的两种经常同时发生的突变引起的。的分子变化这些肿瘤的特征对发现它们的调查人员感到令人惊讶:它们阻止了一种称为枯枝茎的细胞死亡。具有这些变化的癌症要求这一封锁保持活力并增长。该研究发表于2020年12月1日,细胞报告。
铁下垂症是一种依赖铁的程序性细胞死亡。上睑铁下垂被发现不到10年,但它已经成为癌症治疗和其他疾病药物治疗的重要靶点。当下垂铁症没有在应该发生的时候发生时,细胞可以肆意地生长。
“我们真的不知道我们在这些癌症细胞中发现的特殊脆弱性,”胸肿瘤服务主任,Fiona和Stanley Druckenmiller肺癌研究中心的联合主任,胸部肿瘤学局长MSK医师 - 科学家Charles Rudin说本文的高级作者。“但我们在本研究中报告的所有工作指向硬化为关键球员。”
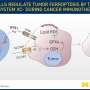
两种突变共同作用
允许癌细胞阻断脱叶菌塞的遗传变化被称为共突变:两个基因的改变,称为STK11和Keap1,共同创造一种环境,其中即使当它们接收到否则诱导的信号时,肿瘤细胞也能够生长的环境细胞死亡。超过10%的肺腺癌存在这两种基因的组合突变,因此一种能够成功靶向这一突变的药物将产生有意义的影响。
MSK BioTTATISTICIAN Ronglai Shen是第一个发现STK11 / Keap1共突然常见于肺腺癌中的肺癌,这是非常侵略性的,难以治疗。在做分析时,她做了发现肺癌症使用来自MSK-ImpactTM的数据,同时在肿瘤中寻找数百次突变的测试。沉博士是新研究的共同作者。
与下垂铁的联系出乎意料。“我们的发现表明,针对某些在调控铁下垂中起作用的蛋白质,可能会导致新的治疗方法。癌症鲁丁博士说。
CRISPR有助于创建有用的实验室模型
在目前的研究中,第一作者Corrin Wohlhieter,一个由Rudin博士和Triparna Sen共同领导的实验室的研究生,使用了基因编辑工具crispr——它允许研究人员对基因编码做出非常具体的改变——创造了三种类型的细胞:有些细胞的STK11基因被敲除,有些细胞的KEAP1基因被敲除,有些细胞的两个基因都被敲除。然后,她将这三种类型的细胞分别分离出来,并在实验室(包括小鼠模型)中进行研究。通过分析细胞的行为,她能够找出当STK11和KEAP1丢失时,哪些其他基因被激活。
“肺癌往往是非常异构的,所以如果你不做这些受控实验,那么很难分离归因于特定基因或一组的变化基因鲁丁博士说。“通过制造这些敲除,我们可以真正关注有这些突变的细胞,并将我们观察到的任何行为与这些因素的存在或缺失联系起来。”
该团队的观察结果帮助他们建立了与骨裂化的联系。他们发现,具有STK11和Keap1突变的细胞也已知具有高水平的蛋白质来使细胞抵抗恶性裂解。Rudin博士和他的同事们发现了其中一种蛋白质,称为SCD1,作为这些肿瘤的特别好的靶标。
“虽然目前的SCD1抑制剂我们不太可能成为良好的药物,”他解释说:“MSK有许多实验室正在积极调查靶向枯萎病的策略癌细胞。"
鲁丁博士说,他计划与其他研究人员合作,进一步了解这些相互作用,寻找可以开发成药物的化合物。他总结说:“我们希望找到抑制这些肿瘤细胞内通路的药物,最终为这些特别困难的癌症开发出一种靶向治疗策略。”










用户评论