机械工程师创建的癌症模型为研究肿瘤生长提供了新的视角
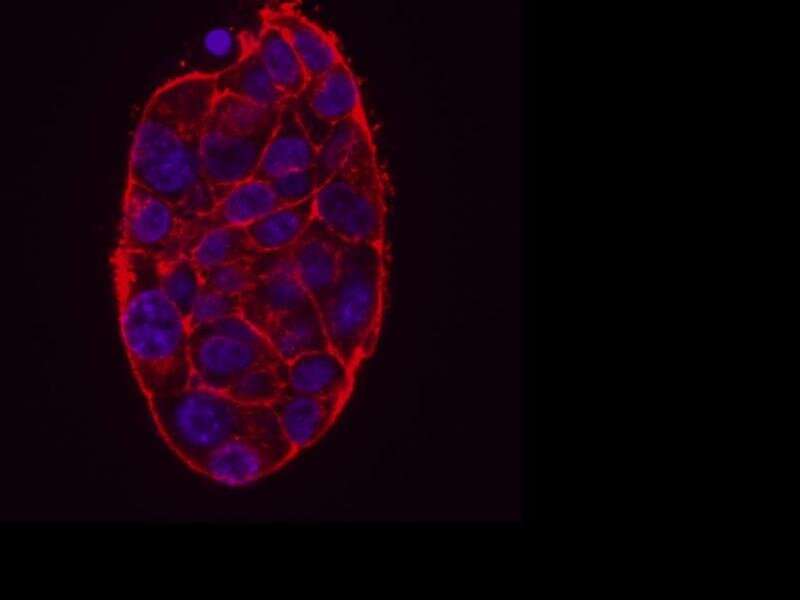
当癌症和肿瘤细胞在人体内移动时,它们会施加机械力,并受其支配。为了了解这些行为是如何影响癌细胞生长、扩散和侵袭的,伦斯勒理工学院的一个工程师团队正在开发新的模型,模拟体内机械环境的各个方面,为肿瘤如何以及为什么以特定方式发展提供新的视角。
在今天发表的研究中综合生物学伦斯勒的一个工程师团队开发了一种体外淋巴系统船研究肿瘤栓塞生长的模型,肿瘤细胞在血管内的聚集经常与增加的转移和肿瘤复发相关。
“肿瘤栓塞的生长对某些癌症的扩散和转移很重要。例如,炎性乳腺癌具有这种增长模式的胚胎在皮肤淋巴管中生长的巨大传播,在乳房中,这是一种非常激进的,“renselaer助理机械工程教授克里斯汀·米尔斯(Rensselaer)担任主教教授,他领导了这项研究。”这种增长肿瘤栓子并没有非常习以很多。“
以前实验室中的肿瘤模型使用的是不受约束的肿瘤细胞球状体,这使得研究人员无法研究管状血管物理边界内真正发生的机械相互作用。为了更接近地模拟体内发生的情况,米尔斯和她的团队在实验室中使用凝胶中的一个小通道来模拟淋巴管。他们将这些通道置于坚硬或柔软的生物惰性凝胶中,以模拟肿瘤栓塞在坚硬的病变组织或柔软的健康组织中可能遇到的约束。
为了整合细胞的不同生长行为,研究小组使用了乳房和结肠癌症细胞聚集在于模拟栓子,一个更具侵略性的栓子,另一个更少。
研究人员发现,僵硬的肿瘤环境模型将两种类型的肿瘤栓子限制在圆柱形通道上,导致栓子沿着血管快速生长。但是,他们发现,根据癌细胞的类型,在模拟健康的结肠或乳房组织的软基质模型中,癌细胞的生长是不同的。
侵袭性细胞完全不受开放通道的影响,呈球形生长,向基质中膨出,而侵袭性较低的细胞首先沿着通道生长数天,然后向基质中膨出。研究人员将生长的差异与癌细胞产生力的能力联系起来。独立的测量表明,侵袭性癌细胞比侵袭性较低的细胞能够发挥更大的力量。
Mills表示,沿着血管或沟道的成长是有问题的,因为肿瘤内的细胞通过血管壁持续进入寿命维持营养物质。当。。。的时候肿瘤细胞米尔斯说,在一个球体中成长,并开始膨胀细胞在那种质量的中心进一步越来越远离营养,直到它们被切断并最终死亡。这些信息对于治疗设计和处方可能是至关重要的。
“我们认为这很重要,因为它以某种方式表明了,如果是瘤这些血管周围的组织已经通过疾病异常加强,或者 - 例如 - 乳房组织已经更密集或更硬,你可能真的看到船只内的增长比柔软的组织更多,“米尔斯也是一个Rensselaer的生物技术和跨学科研究中心的成员。
伦斯勒生物医学工程研究生乔纳森·库尔瓦特诺(Jonathan Kulwatno)是这篇论文的第一作者。米尔斯和库尔瓦特诺与西奈山的研究人员合作。
这种独特的机械工程方法来学习癌症是CBIS在CBIS中进行的变革工作的标志,在那里,像米尔斯这样的研究人员可以与在类似领域的其他工程师和科学家跨学科合作。
CBIS主任迪帕克·瓦什什(Deepak Vashishth)说:“米尔斯教授研究癌症的工程方法奠定了关键的基础,跨学科方法被用于理解癌症的力学生物学,并最终实现治疗目标。”
随着米尔斯和她的团队继续他们的研究,她说,他们正在寻找新的方法使这些模型更加复杂,同时又不丧失分离关键机械机制的能力。
进一步探索












用户评论