欧盟批准第二个冠状病毒疫苗
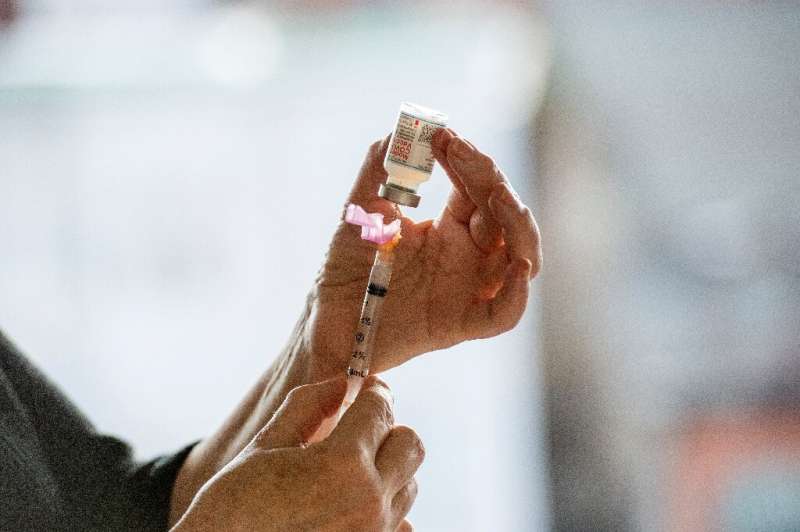
周一的欧盟授权现代冠状病毒刺戳,在速度迅速开始以保护其4.5亿居民后,将Bloc成为第二次疫苗和射击。
第一个迟缓的卷展栏疫苗在欧盟27个国家中,许多国家都在与不断飙升的感染率作斗争。
在总部位于阿姆斯特丹的欧洲药品管理局(EMA)建议对18岁以上人群进行有条件上市批准数小时后,欧洲委员会正式支持了美国公司Moderna的疫苗。
“我们正在为欧洲人提供更多的Covid-19疫苗。随着现代疫苗,第二个现在授权的第二个疫苗,我们将进一步增加1.6亿剂。和更多的疫苗将来,”欧盟委员会首席乌苏拉·沃森·冯德兰说。
欧盟卫生专员Stella Kyriakides表示,Moderna和辉瑞生物科技(Pfizer-BioNTech)疫苗的批准“将确保4.6亿剂疫苗在欧盟加速推出”。
在接种人数方面,欧洲远远落后于美国、英国和以色列。
各国政府一直在向EMA施加压力,EMA将Moderna疫苗的初步会议提前至1月12日周一,但随后表示必须澄清“悬而未决的问题”。
EMA执行董事Emer Cooke在周三再次开会批准该疫苗后发表声明称:“这种疫苗为我们提供了克服当前紧急情况的另一种工具。”
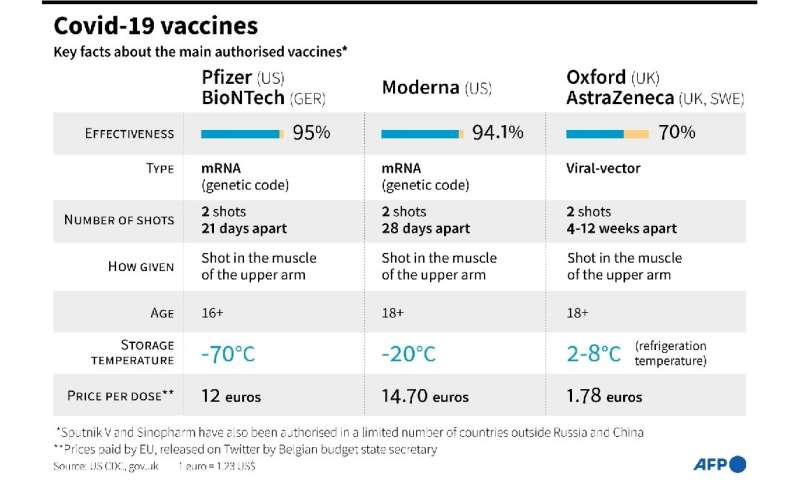
现代疫苗比辉瑞疫苗更容易储存和运输,这需要在减去70℃的温度下保持在冷冻机中,尽管它更昂贵。
EMA为期一年的批准是对Moderna疫苗进行两次注射,间隔28天。
“巨大的挑战”
EMA表示,其人类药物委员会与所有27个国家的专家表示,“彻底评估了关于疫苗的质量,安全性和疗效数据”和建议授权“通过协商一致的资料。
“这将确保欧盟公民,疫苗符合欧盟标准,”它补充说。
欧盟坚持认为,它在使候选人疫苗进行全面的EMA测试协议和与成员国密切协调的最安全的路线,以确定购买和分配多少剂量。
但是,由于他们于12月21日批准,愤怒在疫苗接种疫苗周围避免疫苗的速度缓慢,但愤怒正在增长。
星期三的荷兰成为集团的最终国家。
欧洲理事会主席查尔斯·米歇尔周二晚些时候表示,各国领导人将于本月晚些时候就健康危机举行一次虚拟峰会。
米歇尔说,向欧盟的近4.5亿人提供疫苗是一个“巨大挑战”。
但他坚持认为欧洲委员会是“营业夜间”,以提供更多的疫苗。
Moderna的疫苗在临床试验中被发现有94.1%的有效性,美国已经将其与辉瑞生物科技的疫苗一起使用。
英国正在使用辉瑞和英国制药巨头阿斯利康和牛津大学开发的另一种疫苗。
Ema上周表示,牛津 - 阿里安伦巴疫苗本月不太可能在欧盟批准。
©2021 AFP.












用户评论