肠道感染后,DNA的微妙变化可能易于多发性病变
Guillain-Barré综合征是臭名昭着的自身免疫性神经病变,但遗传变异概述尚未描述这种疾病的个体。在一项新的研究中,来自东京医疗和牙科大学(TMDU)的研究人员在抗体形成免疫细胞制成的蛋白质中发现了两种新的遗传变体,为疾病的发展提供了一种机制。
身体的免疫系统应该争取入侵者;但是,在自身免疫疾病这种防守通过生产自身抗体来骚扰并攻击主机。Guillain-Barré综合征(GBS)是一种急剧开发的自身免疫周围神经病变,导致肌肉无力和麻木。它基于对神经系统细胞膜的特定类型的脂质分子产生自身抗体的基础,这反过来损害了那些神经元并导致多毛细血管。也就是说,对多个外周神经的损伤可能导致肌肉弱点和麻木。GBS通常在免疫刺激之前,例如感染。实际上,用细菌弯曲杆菌的感染延伸,导致腹泻病,是GBS发展之前最常见的事件。然而,由于并非所有患有这种细菌疾病的患者随后开发GBS,它已经渴望思考遗传变异(个体之间的DNA差异)可能是促使患有GBS的患者对多肺病变的患者。
“GBS仍然有点医疗谜团。我们不完全理解为什么患者培养这种疾病,”研究教授Takeshi Tsubata教授的相应作者说。“我们的研究的目标是鉴定GBS患者的遗传变异,并为生产这些患者的多种疾病的发育提供自身抗体的潜在机制。”
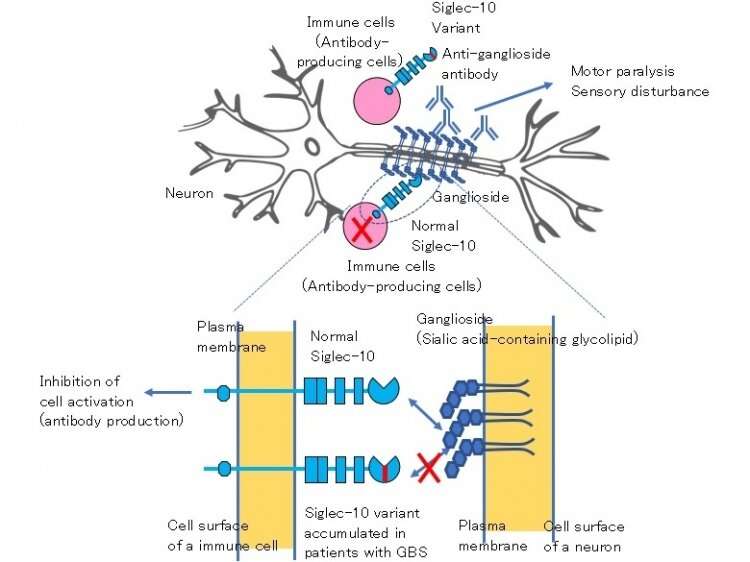
为了实现他们的目标,研究人员集中在蛋白质Siglec-10上。SigleC-10由B淋巴细胞产生,一种产生抗体的特定类型的免疫细胞,并与神经节苷脂结合。研究人员假设Siglec-10可能在抗神经节苷脂的抗体的生产中起到抑制作用,并且依次在Siglec-10中的遗传变异可以减少这种抑制作用,从而促进GBS的发育。通过分析GBS患者蛋白质Siglec-10编码的DNA序列,研究人员确定了两种改变的罕见变体氨基酸序列在GBS患者的蛋白质中。没有两个变体中只有一个的患者可能是因为这两个变体位于SigleC-10基因中非常紧密。
然后,研究人员在实验室中制备了GBS特异性SigleC-10蛋白,以了解它在分子水平下如何与正常的Siglec-10蛋白质不同。他们发现,两个变体中只有一种对交替蛋白的有害作用负责,导致蛋白质的分子结构和蛋白质的显着变化,以结合神经节。
“这些是显着的结果,展示了Siglec-10如何抑制神经节苷脂的抗体产生,并且轮到变种方式蛋白质可能倾向于突出的发作症综合征的发展。这些发现有助于我们了解该疾病的病理生理学,“研究Amin alborzian Deh Sheikh第一个作者说。
进一步探索











用户评论