STING激活减少小鼠模型中的移植物抗宿主疾病
MUSC Hollings癌症中心研究员吴永霞博士发现了一种新的靶向分子对抗移植物抗宿主病(GVHD)。骨髓移植是治疗某些血癌的一种方法,在将近50%的患者中伴随着潜在的危及生命的GVHD。2021年1月发表于细胞与分子免疫学揭示了激活一种叫做STING的分子可能是一种减少GVHD的新方法。
于学忠,医学博士,微生物与免疫学教授,专注于理解调节GVHD发育和抗肿瘤活性的复杂免疫机制。
近年来,STING(干扰素基因刺激因子)在癌症研究中得到了高度重视。其他组的数据显示,T细胞帮助免疫细胞对抗癌症。癌细胞本质上是人体自身细胞的“坏”版本,是其适当的目标免疫系统。相反,在移植物抗宿主病中,T细胞对抗身体自身的“好”细胞——本质上,身体攻击自己。根据之前的数据,高剂量的STING激活虽然对癌症有益,但在GVHD的背景下却是有害的,这似乎合乎逻辑。Yu在GVHD小鼠模型上的发现证实了这一假设。小鼠模型由合作者Chih-Chi Andrew Hu博士(Wistar Institute的病理学和检验医学教授)获得,GVHD是由骨髓移植诱导的,这与人类的疾病发展密切相关。
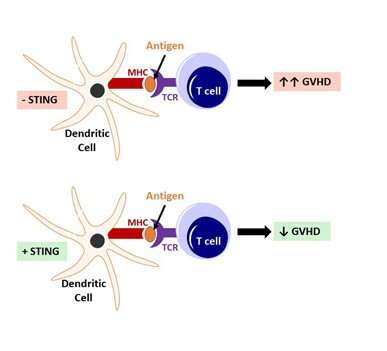
了解GVHD是如何发展的骨髓移植在美国,必须考虑两种免疫系统:供体免疫系统和受体免疫系统。关键的免疫细胞是抗原提呈细胞和T细胞。免疫系统根据被称为抗原的特定“标签”,知道该攻击什么,这些“标签”由专门的抗原呈递细胞显示给T细胞。树突状细胞是最有效的抗原提呈细胞,在移植物抗宿主病中起着关键作用。
其他癌症研究小组的工作已经证明STING信号可以调节抗原提呈细胞的功能。STING是导致炎症细胞因子产生的dna传感通路中的一个重要分子。但目前尚不清楚STING在移植物抗宿主病中是如何调节这些细胞的。
研究人员使用小鼠模型来确定当STING在供体免疫细胞中缺失,受体免疫细胞中缺失和受体免疫细胞中过表达时,移植物抗宿主病是改善还是恶化。当STING不在供体免疫细胞中时,GVHD的严重程度没有改变。然而,当STING从受体中消失时,GVHD更严重,死亡率更高免疫细胞。
Yu和他的合作者研究了不同的细胞亚群,试图了解哪些细胞受STING损失的影响最大。令人惊讶的是,受体小鼠的抗原提呈细胞(树突状细胞)中STING的表达减少了骨髓移植后供体T细胞的扩张和迁移能力。换句话说,它降低了受体小鼠的T细胞攻击其“好”细胞并导致GVHD的可能性。这一发现被一种能开启STING分子的药理学药物所证实。移植前在宿主体内激活STING可降低GVHD的严重程度。
在一个小鼠模型用药理药物激活STING可以降低GVHD,这可能与临床相关,这表明STING激活药物可能保护GVHD骨髓移植受者移植物抗宿主病。更基本的临床研究将被要求评估这种可能性,但于的发现表明,这样的研究是有根据的。
为了理解为什么研究小组观察到他们所做的,他们将继续解开STING分子的生物学功能。悬而未决的问题包括,是什么使STING在不同的免疫细胞亚群中功能不同。
“我们合作者的老鼠等工具使我们能够更彻底地研究这一问题。一种蛋白质的全体删除不允许在细胞亚群中进行特定的研究,我们认为STING一定在不同的细胞中有不同的作用,”Yu解释道。













用户评论