化疗后的骨髓如何再生
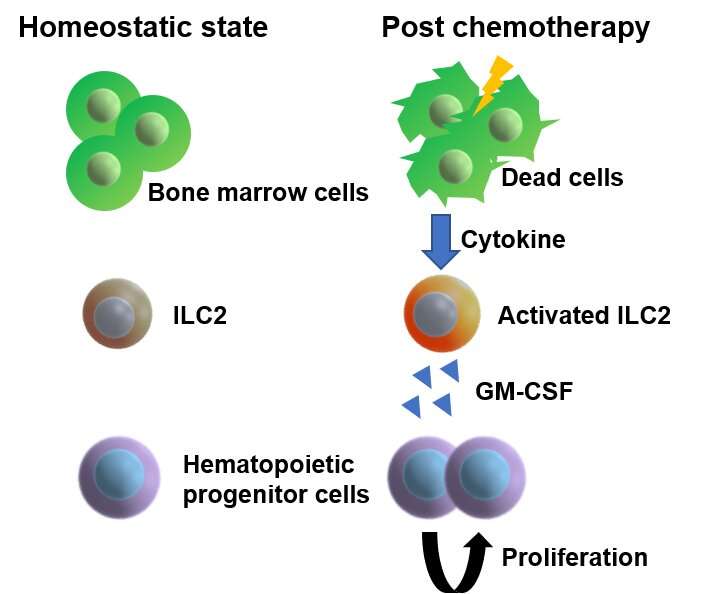
化疗对骨髓中的造血干细胞和祖细胞(hspc)具有破坏作用。然而,一旦化疗结束,热休克细胞会再生,这一过程至今仍是未知的。在一项新的研究中,大阪大学的研究人员发现了热休克细胞损伤后恢复的分子机制。
热休克细胞存在于骨髓中,产生多种类型的血细胞,例如红细胞(携带氧气),一些白细胞(对此很重要免疫系统)和血小板(止血所必需的)。由于热休克干细胞不断分裂产生新的细胞,它们对化疗等引起的损伤特别敏感。有趣的是,热休克干细胞具有损伤后再生的能力。
“骨髓是一个非常活跃的器官,因为它必须不断产生新的血细胞,”研究Masaru Ishii的相应作者说。“一旦它失去其功能,例如在化疗期间,可能会发生贫血,中性粒细胞病和出血的致命条件。在这项研究中,我们想了解如何造血词根骨髓中的细胞会在化疗引起的损伤后再生,以恢复其全部功能。”
为了实现他们的目标,研究人员专注于由Hspcs,所谓的第2组先天淋巴细胞(ILC2S)产生的特定血细胞血细胞子集。虽然ILC2在许多组织中存在并在免疫系统和组织修复中发挥重要作用,但仍被认为具有特定于其位置的不同作用。然而,他们的功能的性质尚不清楚。为了揭开ILC2S的生物学作用,研究人员用5-氟尿嘧啶(5-FU),化学治疗剂对Hspcs有毒的小鼠进行处理,并将新鲜的未被未润润的Hspcs移植到这些小鼠中,类似于白血病患者的干细胞移植治疗。有趣的是,研究人员发现,5-FU处理的小鼠中受损的HSPC微环境促进移植的HSPC的增殖。通过分析这一发现分子水平上,研究人员发现,治疗小鼠骨髓中的ilc2产生粒细胞-巨噬细胞集落刺激因子(GM-CSF),以协助HSPC的再生过程。
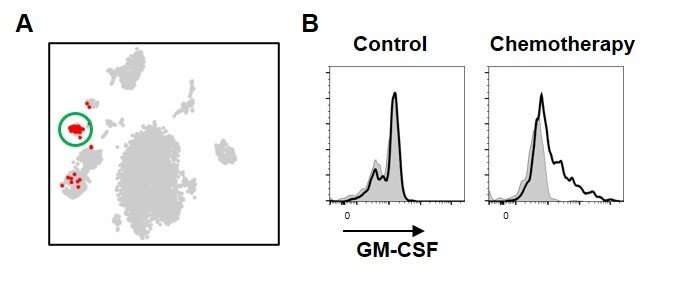
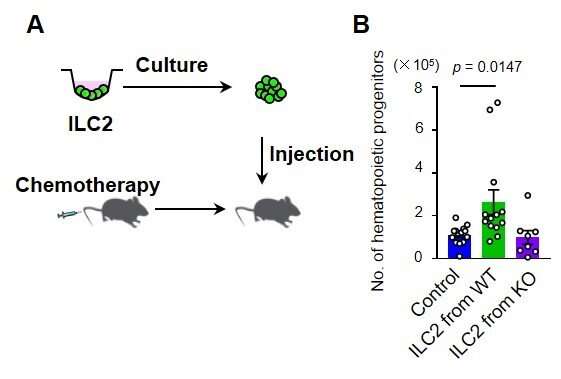
但是,ILC2的究竟是如何在骨髓受伤后产生GM-CSF的?为了回答这个问题,研究人员扩大了他们的重点,以调查是否有其他细胞或分子直接ILC2-生产GM-CSF。他们发现,在骨髓中产生的抗体产生的B细胞的祖细胞在损伤后产生了白细胞介素(IL)-33,这反过来活化ILC2S,证明了如何回收损坏的骨髓。重要的是,研究人员表明,分离的ILC2S转移到5-FU处理的小鼠加速造血回收率,同时降低ILC2S的效果相反,表明ILC2可以用作骨髓损伤的传感器。
“这些都是显着的结果,表明了骨髓化疗后再生,“研究的第一个作者Takao Sudo。”我们的结果可能有助于开发一种新型化疗诱导的肌球瓶抑制的治疗方法。“
本文,“2组先天淋巴细胞支持在压力条件下造血回收,”发表在实验医学杂志。
进一步探索













用户评论