癌症的“监护人”与一个交换机打破了糟糕
在有效的肿瘤抑制蛋白中取代单个氨基酸的突变将其从Saint转变为阴性。德克萨斯州机构联盟的一项新研究表明,为什么比以前所知的更具损害。
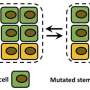
普遍存在的P53.蛋白质在其自然状态下,有时称为“基因组的监护人”,是一个反对的前线保护器癌症。但突变形式出现在50%以上人类癌症并积极阻断癌症抑制器。
Peter Vekilov在休斯顿大学(UH)和赖斯大学的Anatoly Kolomeisky领导的研究人员发现了同样的突变蛋白可以聚合到集群中。这些反过来成核,形成淀粉样蛋白原纤维,癌症患者的主要嫌疑人以及神经疾病像阿尔茨海默里的。
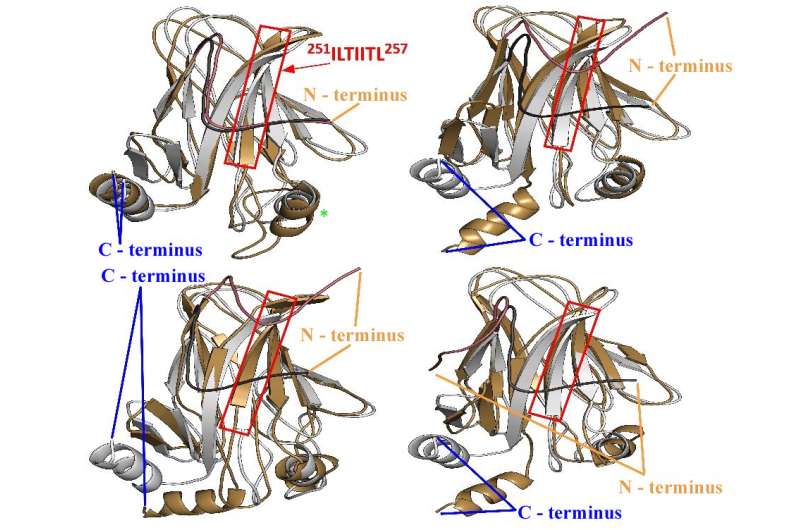
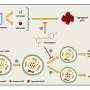
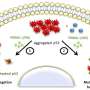
它们报道,当单个精氨酸氨基酸被谷氨酰胺取代时,通过蛋白质的DNA结合口袋的稳定化驱动P53变成簇的凝结。
“众所周知,该蛋白质中的突变是癌症的主要来源,但机制仍然是未知的,”大米化学系教授和化学和生物分子教授的教授和椅子的机制仍然是未知的。
“这种知识差距显着限制了控制聚集和建议新型癌症治疗的企图,”韦科洛夫,约翰和丽贝卡·摩尔人在呃,化学和生物分子工程和化学教授。
突变体P53簇,其20多年前在其他蛋白质溶液中发现的vekilov那些,以及它们核心的淀粉样蛋白原纤维促使蛋白质的聚集体用于抑制癌症。“这类似于神经系统疾病中大脑发生的事情,尽管这些疾病是非常不同的疾病,”Kolomeisky说。
vekilov表示,国家科学院院长中描述的P53机制可能与模块,长丝,镰状细胞聚合物,淀粉样蛋白和晶体等功能和病理固体相似。
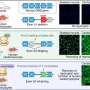
UH组合的研究人员在化学和生物分子工程师Navin Varadarajan实验室中携带的乳腺癌细胞3D共聚焦图像,具有vekilov实验室中纯化蛋白质的光散射和光学显微镜。
在加尔维斯顿(UTMB)的德克萨斯州德克萨斯大学(UTMB)的Michael Sherman贡献的簇电子显微镜显微镜显微镜和母纤维形成由康沃尔群岛群岛的主要结果支持了该研究的主要结果
所有证实称为R248Q的P53突变体通过两步方法以形成瞳孔透视凝聚物。Vekilov表示,了解该机制可以欣赏治疗操纵P53或其相关的信号通路的各种癌症。
在正常的细胞条件下,P53的浓度相对较低,因此聚集的概率低,他说。但是当存在突变的P53时,概率增加。
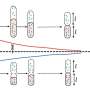
“实验表明,这些簇的尺寸与P53的浓度无关,”Kolomeisky说。“突变的P53甚至将正常的P53将p53纳入聚集体。这是称为功能损失现象的原因之一。”
据研究人员称,如果存在突变体的突变体的小相对部分,则足以杀死或降低正常野生型P53的能力。
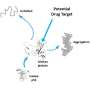
水稻模拟显示正常的P53蛋白质是紧凑的,并且容易与DNA结合。“但是突变体具有更开放的构象,使它们与其他蛋白质相互作用,并给予它们较高的产生冷凝物的倾向,”洛格洛梅斯说。“未来的抗癌药物可能会以抑制这些聚集体的形成的方式靶向突变体,并允许野生型P53进行工作。”
进一步探索









用户评论