在严重的视觉障碍上恢复时钟
Gustavo Aguirre和William Beltran,宾夕法尼亚州兽医大学兽医学院的兽医眼科医生和视野科学家研究了各种不同视网膜掩饰障碍。但是NPHP5基因突变引起的一种导致Leber先天性半衰期(LCA)的形式是最严重的。
“这种疾病的孩子们不视觉,”Aguirre说。“他们有一个徘徊,搜索在他们的脸上,通常在年轻时被诊断出来。”
几乎相同疾病自然发生在狗身上。在期刊的新论文中分子治疗,宾夕法尼亚州和其他机构的Aguirere,Beltran和同事表明了一个犬类基因治疗可以恢复正常结构和功能到视网膜的锥体感光体细胞,其中,在LCA患者中,否则无法正常发展。在治疗的狗中提供NPHP5基因恢复的犬或人文版的正常副本。
“有什么惊人的是,你可以服用这种疾病锥形细胞已经不完全形成,治疗恢复了它们的功能 - 它们在恢复之前没有任何功能,“Aguirre说。
“这种可塑性令人难以置信并给予我们很多希望,”贝尔特兰说。
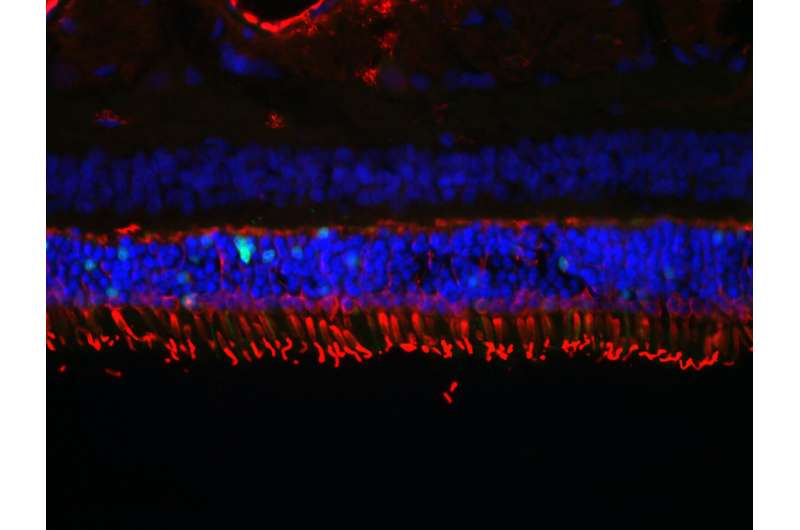
LCA包括广泛的遗传视觉障碍,其特征在于童年的失明。与NPHP5突变相关的LCA的形式罕见,影响全世界约5,000人。被称为纤毛病,它影响了纤毛细胞视网膜。纤毛细胞是在感光体细胞上的抗体摩擦结构,其将能量从光转化为可视信号。
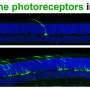
在NPHP5疾病中,杆光感受器细胞 - 负责低轻质退化和逐渐死亡的视力的人。然而,锥形光感受器能够实现颜色视觉,在中央视网膜中,对细节的感知,同时在结构上异常,存活,尽管没有功能。
Aguirre和Beltran与Conteagues和Samuel Jacobson在Penn的Perelman医学院的同事和同事一起,已找到成功的基因治疗方法,治疗各种遗传性视觉障碍。通常,在感光体细胞死亡或完全退化之前,他们旨在在视网膜疾病过程中治疗。但是,锥体细胞以这种形式的LCA持续存在的事实导致研究人员考虑靶向锥体的治疗是否无法停止,但扭转疾病的过程。
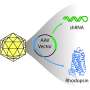
测试这种方法,该团队随着腺相关病毒载体的视网膜注射,一个平台,用于将正常版本的NPHP5基因融合成九个五周龄犬的一只眼睛,具有视力障碍。被称为基因增强治疗,注射用于在疾病中提供健康基因,其中致病性突变导致缺陷或不存在蛋白质。
为了确定治疗的有效性,研究人员使用称为电动图级别的技术,该技术测量光感受器细胞对光刺激的电响应,以及光学相干断层扫描,这允许视网膜的细横截面的非侵入性成像。评估实验疗法的两种方法使令人鼓舞的结果。在狗的治疗眼睛中,锥体的外部段重新进行重新重新。
此外,当治疗的狗大约六个月大时,他们想象使用障碍避免课程进行了测试。当他们的治疗眼睛被蒙住眼睛时,它们难以导航;然而,当揭开这种眼睛时,他们避免障碍物的能力是显着的改善。
“这是如此令人吸引人,如此令人兴奋的是,我们不仅仅是停止疾病过程,我们实际上是恢复了一个感光器蜂窝是变得正常和功能的,“Beltran说。”这种疾病在狗的疾病非常紧密地在人类的疾病中,在相当具体的术语,因此有很多人的支持,认为类似的治疗方法也可以帮助孩子。“
正在进行的研究表明,即使在疾病的后期阶段交付时,治疗也可能是有效的。通过进一步的支持,研究人员希望沿着人们临床试验的道路移动研究。
进一步探索









用户评论