发现对病毒肺感染的新防御
研究人员已经发现了一个先前未知的免疫防御系统手臂,保护肺部免受致死病毒感染。
由病毒如流感A和SARS-COV-2引起的呼吸系统疾病导致损坏不仅仅是通过自己的行为,而且造成抵押品损害,因为免疫系统对抗感染作出反应。
及时和比例的反应鉴定病毒,将它们与吞噬物质的微小囊泡隔离,然后靶向击穿。该过程触发细胞因子的产生以提醒免疫系统。
细胞因子响应代表一种精细平衡行为,有时可以将其倾斜到称为细胞因子风暴的过度状态。这对病毒肺感染具有严重后果,因为它导致炎症,肺部液体和最终死亡。
鉴于呼吸状况的影响,通过Covid-19大流行引起敏锐的重点,清楚地需要充分了解这种免疫反应的复杂性,以发展能够保护持有的感染的药物的更好的治疗或靶标。
从Quadram Institute和Liverpool大学致辞,东安格利亚(UEA)和布里斯托尔致力于研究对流感的免疫反应病毒在小鼠的肺部感染。动物模型提供了一种理解的方式免疫系统作品,与SARS-COV-2一样,动物可能是一个重要的水库,用于病毒,如果转移到人类,可以引发流行病。
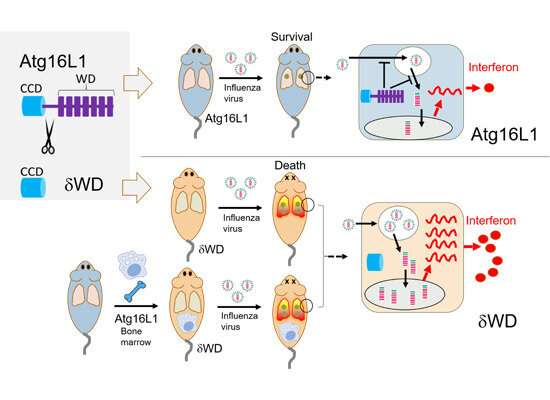
由生物技术和生物科学研究委员会资助,他们专注于最近表征的非规范自噬作用形式,称为LC3-相关吞噬作用(LAP),其识别出在进入细胞的病原体。
汤姆威尔曼教授在Quadram Institute曾与佩尼·鲍威尔博士和UEA教授均致电,以开发缺乏鼠标以研究病毒感染。本研究的独特之处,小鼠设计用于保留正常的自噬机械,并在免疫细胞内靶圈,了解这一新发现的免疫防御的精确作用的最佳选择。
利物浦大学詹姆斯·斯图尔特教授通过感染具有流感病毒的转基因小鼠并研究对感染的反应来表征圈的功能。
发现小鼠更容易受到病毒的影响,用它引发导致肺炎的细胞因子风暴。研究人员表明,通过抑制肺炎,膝盖阻止了致命的细胞因子风暴。
那么这种保护来自哪里?Yohei Yamauchi博士和布里斯托大学的同事通过看衬里表面的细胞来提供答案。病毒如何最初与这些细胞结合,但他们确实看到非规范的自噬/圈确实缓慢了病毒进入细胞的方式。它可以通过防止具有内体的病毒融合,这是从外部进口材料的细胞。
非典型自噬/圈可能与第一次防范很重要感染,在此之前没有免疫感染,特别是在流感和SARS-COV-2的特定情况下。
“能够描述这种小说的免疫防御系统免受呼吸道感染的非常令人兴奋,特别是鉴于目前的大流行,”来自东安格利亚大学的汤姆威尔曼教授汤姆威尔曼教授。
“我们需要评估同一系统是否在人类中提供类似的保护,但这确实指出了开发制动这种非规范自动的新药物以增加阻力的可能性肺表面,最需要的地方。“










用户评论