非处方家庭COVID-19检测获得紧急批准
美国食品和药物管理局上周授予紧急使用授权(EUA)两次在家试验,以检测严重的急性呼吸综合征冠状病毒2(SARS-COV-2),包括第一个不需要处方的家庭测试。
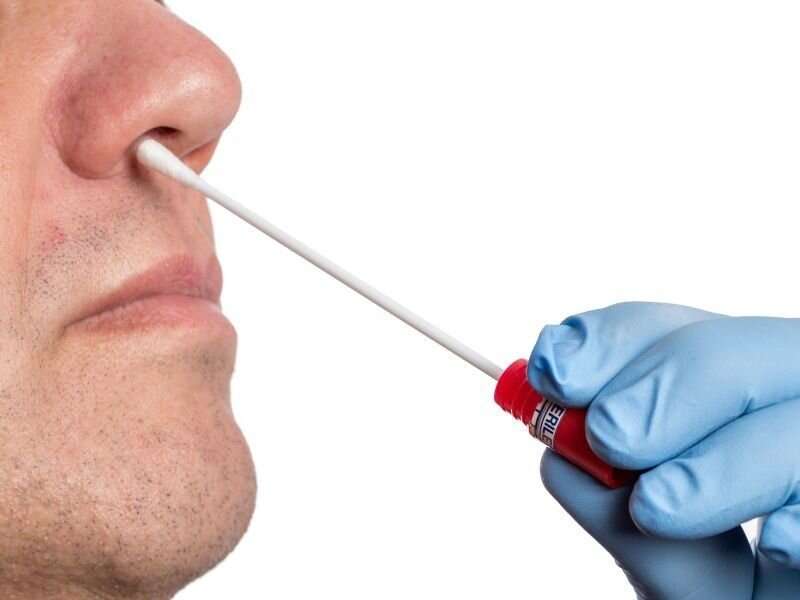
周五,该机构宣布了家庭和柜台上的提示Covid-19试验的EUA(OTC)使用,旨在从鼻拭子标本中的SARS-COV-2检测遗传物质的分子核酸扩增试验。该测试被授权在成人和2岁及以上的成人被成年人发出的年长的成人使用的非专利人士。它可以用于有或没有症状的个体。
测试包包括鼻拭子,测试墨盒,测试墨盒阅读器和移动应用程序。墨盒阅读器运行测试墨盒,并在大约20分钟内将结果传递给移动应用程序。数据显示,新冠肺炎居家和OTC检测对有症状人群的阳性样本正确率分别为96%和100%。Cue Health表示,预计到今年夏天,该公司每天将进行超过10万次测试。
上周,FDA为Quidel Quickvue颁发了Quidel Quickvue-19考试的EUA,一种抗原试验,用于在14岁及以上的人和8岁及以上的儿童和超过8岁及以上的儿童的自集前鼻拭子拭子由成年人收集。这测试被授权适用于他们的个人卫生保健提供者在出现症状的6天内发现疑似COVID-19。
FDA现已授权超过330个测试和收集套件,用于检测SARS-COV-2。"The FDA will continue to expand Americans' access to testing to help us in the fight against this pandemic, which has claimed over half a million lives in the United States," Acting FDA Commissioner Janet Woodcock, M.D., said in an agency news release.
版权所有©2020.每日健康。保留所有权利。













用户评论