令人惊讶的是,一些阿尔茨海默氏病的斑块可能是保护性的,而不是破坏性的
阿尔茨海默病(AD)的一个特征特征是大脑中淀粉样蛋白斑块的积累。大多数治疗阿尔茨海默病的疗法都是针对这些斑块,但在临床试验中大部分都失败了。索尔克大学的科学家们进行的一项新研究颠覆了人们对一种常见斑块起源的传统看法,揭示了治疗不成功的原因。
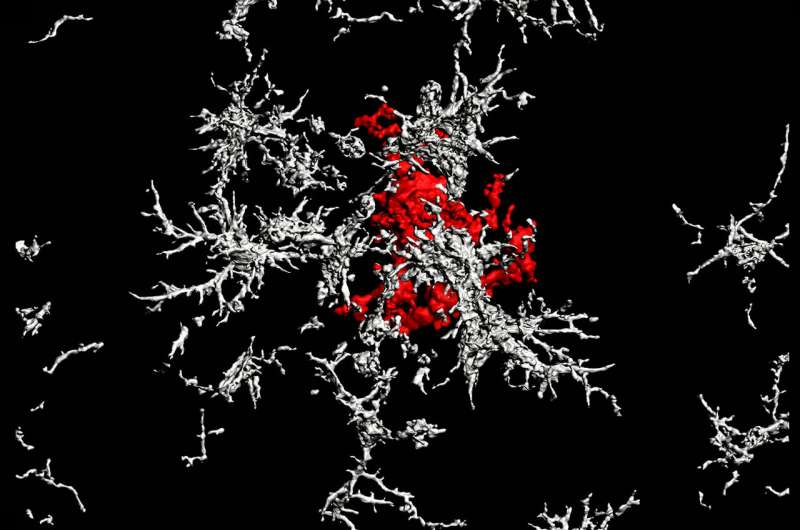
传统观点认为,大脑的垃圾清理免疫细胞,被称为小胶质细胞,通过“进食”来抑制斑块的生长。Salk科学家们表明,小胶质细胞促进了密集核心斑块的形成,并且该动作扫除了蝇斑的材料,远离神经元,其中导致细胞死亡。研究,发表在自然免疫学2021年4月15日,暗示密集核心斑块发挥保护作用,因此摧毁它们的治疗可能比善得更好。
“我们表明,高密度核心斑块不会自发形成。我们相信它们是由小胶质细胞形成的一种防御机制,所以最好不要管它们,”索尔克分子神经生物学实验室的教授格雷格·莱姆克(Greg Lemke)说。“为了让FDA批准其主要临床效果是减少致密核心斑块形成的抗体,我们做出了各种努力,但我们认为,打破斑块可能会造成更大的损害。”
阿尔茨海默病是一种神经系统疾病,会导致记忆丧失、思维障碍和行为改变,随着我们年龄的增长,这些症状会恶化。这种疾病似乎是由大脑之间异常的蛋白质聚集引起的细胞要形成标志性斑块,可保持细胞活着的中断活动。
有许多形式的牙菌斑,但是最普遍的两个是“漫反射”和“密集核”的表征。弥漫斑块松散地组织,无定形云。密集核心斑块设有一个由光环包围的紧凑型中心。科学家们普遍认为,两种类型的斑块形式从过量产生前体分子的过量产生淀粉样蛋白前体蛋白(应用程序)。
但是,根据新的研究,它实际上是从弥漫淀粉样蛋白 - β原纤维形成致密核心斑块的小胶质细胞,作为其细胞清除的一部分。
这是一个建立在一个2016年发现由LEMKE实验室确定当脑细胞死亡时,脂肪分子从内部翻转到细胞外部,发信号前,“我死了,吃掉我。”在称为Gas6的中间分子的帮助下,通过称为TAM受体的通过表面蛋白质,吞噬或“吃”死池。没有TAM受体和Gas6,Microglia无法连接到死细胞并消耗它们。
研究小组目前的工作表明,不仅是死细胞表现出吃我的信号和气体,阿尔茨海默病中普遍存在的淀粉样斑块也是如此。使用动物模型,研究人员能够第一次实验证明,具有TAM受体的小胶质细胞通过eat-me信号和Gas6进食淀粉样斑块。在缺乏TAM受体的小鼠中,小胶质细胞无法执行这一功能。
挖掘更深,他们使用实时成像跟踪了密集核心斑块。对于他们的惊喜,团队发现,在微胶质细胞吃弥漫性斑块之后,它将据蛋白淀粉样蛋白β转移到高度酸性室中并将其转化为高度压实的聚集体,然后将其转移到致密核斑块中。研究人员提出这是一种有益的机制,组织弥漫核斑块并清除碎片的细胞间环境。
“我们的研究似乎表明,当密集核心斑块较少时,似乎似乎有更有害的影响,”纸上的第一个作者说。“随着更多弥漫的斑块,有丰富的营养不良神经肌层,是神经元损伤的代理。我不认为这是一个不同的临床决定,斑块的斑块或多或少有害,但通过我们的研究,我们似乎找到了密集的核心斑块有点良好。“
他们的研究结果表明了开发阿尔茨海默病治疗的新方法,例如促进TAM受体对小胶质细胞的表达,以加速密集核心牌匾形成。研究小组希望进行认知研究,看看增加小神经胶质TAM受体的活性是否可以减轻AD的影响。
持有FrançoiseGilot-Salk主席的Lemke认为,大多数阿尔茨海默氏药物试验的失败率即将结束。“有些人说,试验的相对失败摧毁了密集的核心斑块反驳了淀粉样蛋白β在大脑中是坏事的想法,”莱姆克说。“但我们认为淀粉样蛋白β仍然显然是一件坏事;只是你必须问密集的核心斑块是坏事。”
莱姆克建议,寻找阿尔茨海默氏症治疗方法的科学家应该停止把注意力集中在分解致密核心斑块上,而是开始寻找一种治疗方法,要么首先减少淀粉样蛋白的产生,要么促进淀粉样蛋白从大脑中运输出去。














用户评论