阿斯利康和强生疫苗的血块问题
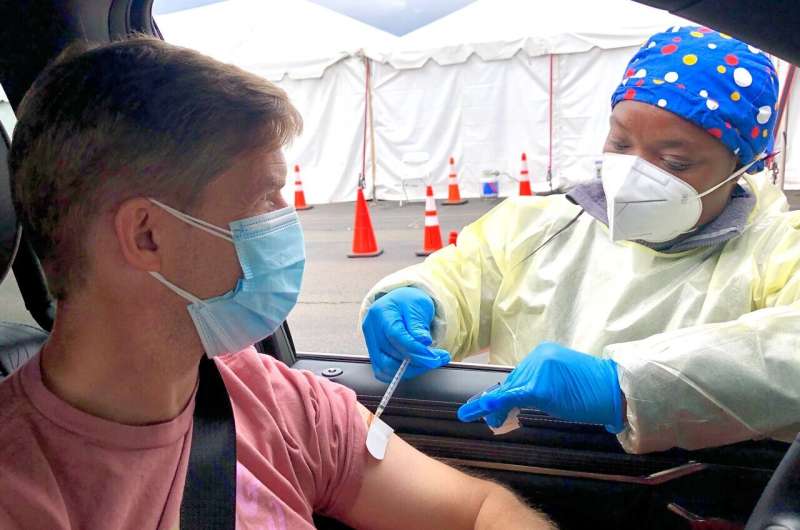
阿斯利康(AstraZeneca)和强生(Johnson & Johnson)的疫苗被怀疑在少数病例中导致非常罕见但严重的血块。在控制疫情的努力中,数百万人接种了疫苗。
以下是我们对这两种疫苗的了解,它们基于相同的技术。
发生了什么事?
欧洲药品管理局上周表示,不寻常的血凝块应该被列为阿斯利康非常罕见的副作用疫苗他强调,预防COVID-19的总体效益大于风险。
凝块出现在大脑的静脉中,称为脑静脉窦血栓形成,以及腹部和动脉。
它们的罕见之处不仅在于它们在体内的出现,还在于它们与帮助血液的低水平血小板一起出现凝块。
矛盾的是,这可能意味着病人同时有出血和血栓。
根据EMA的数据,截至4月4日,在欧洲经济区(欧盟、冰岛、挪威、列支敦士登)和英国进行的3400万例阿斯利康注射中,有222例非典型血栓。截至3月22日,已有18人死亡。
报告的大多数病例发生在接种疫苗两周内的60岁以下妇女中。
在美国,超过680万次的强生单针疫苗注射已经实施,卫生当局周二建议暂停注射,因为他们正在调查6例报告的CVST病例,这些病例也发生在血小板水平较低的情况下。
官员们说,所有这些病例都涉及年龄在18到48岁之间的女性,其中有一例死亡。
怀疑的原因
这两种疫苗——以及俄罗斯的Sputnik V疫苗——都是基于一种被称为“病毒载体”的技术。
疫苗使用常见的引起腺病毒,修改所以它无法复制,作为梭语遗传指令的“载体”人类细胞让他们创造一种冠状病毒的蛋白质。
阿斯利康选择了黑猩猩腺病毒,强生选择了人类腺病毒。
“虽然某些COVID-19疫苗之间的因果关系,血小板异常和血凝块,到目前为止,被证实,怀疑是指数上升,这些罕见的情况下可能引发的腺病毒组件的阿斯利康和强生疫苗,”埃莉诺·赖利说,爱丁堡大学免疫学教授。
机制是什么?
尽管尚无任何证据,但美国食品和药物管理局(fda)的彼得•马克斯(Peter Marks)表示,血栓的“可能原因”可能是对疫苗的不寻常反应。
FDA还表示,在正常情况下,一种叫做肝素的抗凝血药物会用于治疗这些疾病血血栓,在这种情况下,使用肝素可能是危险的。
这可能是因为这种疾病类似于肝素本身的罕见反应,其中体内形成抗体响应于较薄,并且又触发血小板以形成危险凝块。
今年3月,一个由德国和奥地利科学家组成的团队发现了这种先前已知的肝素免疫反应与阿斯利康疫苗之间的联系。
EMA说这是“一个合理的解释”,并呼吁进行更多的研究。
平衡风险
该欧洲机构表示,尚未证实阿斯利康疫苗出现这种反应的特定风险因素,但不同国家选择了按年龄限制接种。
其理由是,年龄越大的人,就越有可能患上严重的COVID - 19,而且接种疫苗也就越符合他们的利益,尽管有潜在的副作用。
例如,英国已表示,30岁以下的患者不会使用阿斯利康,而55岁以下的患者法国则不使用。
在美国,卫生当局表示,暂停强生疫苗是“出于谨慎”。
在过去三周内注射过疫苗的人被要求在出现严重头痛时向医生报告,腹部疼痛,腿部疼痛或呼吸急促。
伦敦卫生与热带医学院(London School of Hygiene & Tropical Medicine)药物流行病学教授伊恩·道格拉斯(Ian Douglas)表示,强调这些事件看起来有多罕见是很重要的。
“从这个角度来看,这与英国任何一年被闪电击中的几率相似,”他在回应美国的声明时告诉科学媒体中心。
“另一方面,新冠肺炎带来的风险是巨大的。”
©2021法新社
















用户评论