欧盟审查强生血块链接,扩大阿斯利康的调查
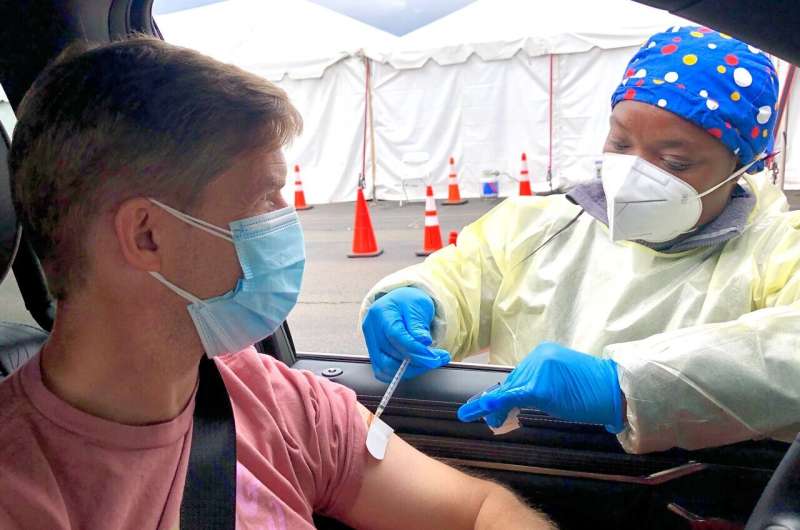
欧盟药品监管机构周五表示,正在审查强生冠状病毒疫苗注射患者可能出现的血栓病例,并调查一种与阿斯利康疫苗有关的新情况。
欧洲药品管理局(EMA)在一份声明中说,在接种强生疫苗的人群中报告了四例罕见的低血小板凝块病例,其中一例死亡。
与此同时,据报道,有5例患者在接受阿斯利康的注射后出现了一种罕见的情况,即微小的血管发生泄漏,导致肿胀和血压下降。
位于阿姆斯特丹的EMA在一份声明中表示,目前尚不清楚两种疫苗和这些病例之间是否存在因果关系。
本周三,监管机构宣布将血液凝块列为英国-瑞典联合公司阿斯利康(AstraZeneca)注射的一种非常罕见的副作用后,有关疫苗安全性的新问题就出现了。
但EMA表示,其安全委员会现在已将注意力转向美国制药巨头强生公司,并“开始对注射疫苗的人的血栓栓塞事件报告进行评估”。
他说:“在临床试验中出现一例病例,在美国推广疫苗期间出现三例病例。其中一人是致命的。
EMA已经批准强生公司的疫苗投入使用,但其在欧盟27个国家的推广要到本月晚些时候才会开始。
强生公司表示,在接种疫苗后发生了“少量非常罕见的事件”。
该公司在一份声明中表示:“目前,这些罕见事件与Janssen COVID-19疫苗之间尚未建立明确的因果关系。”Janssen是强生欧洲子公司的名称。
与此同时,EMA安全委员会也开始审查欧洲接受过阿斯利康疫苗接种者的“毛细管泄漏综合征报告”。
报告称:“已经报道了5例这种非常罕见的疾病,其特征是血管渗出液体,导致组织肿胀和血压下降。”
强生和阿斯利康的疫苗都使用了类似的腺病毒载体技术。
EMA表示,在对两份新报告进行调查后,它将“决定是否有必要采取监管行动”,这通常包括添加一份关于副作用的通知。
EMA本周早些时候表示,他们已经知道了与强生疫苗有关的病例,但给出的数字较低,仅为3例,并没有提及死亡。
EMA安全主管Peter Arlett在周三的新闻发布会上表示,与强生公司在全球范围内注射的450万针相比,这一总数“非常小”。
“然而,这正受到密切关注……我认为,公平地说,在所有疫苗中都对这一问题进行了严密的监测。”
他补充说,全世界也有35例与辉瑞生物技术疫苗有关的血块病例报告,5例与Moderna疫苗有关。
进一步探索
©2021法新社










用户评论