肌肉萎缩症治疗中的一个里程碑
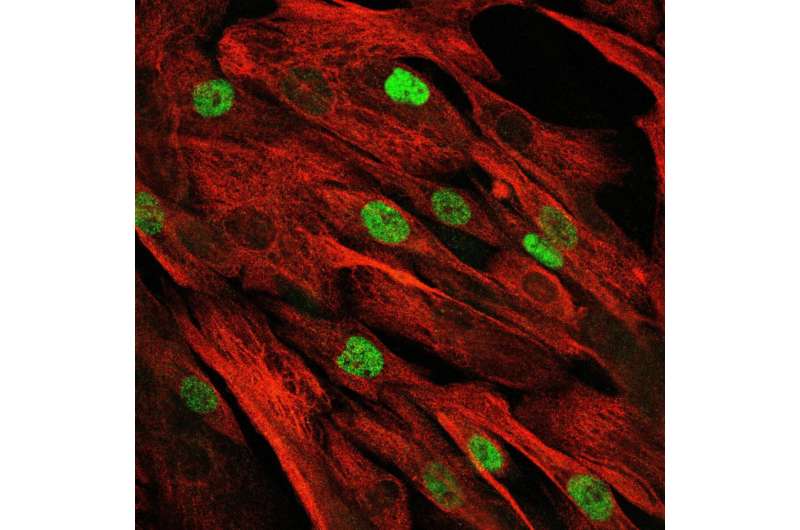
肌肉干细胞使我们的肌肉能够通过运动来建立和再生。但是,如果某些肌肉基因发生突变,则发生相反的情况。在患有肌营养不良症的患者中,骨骼肌已经开始在儿童时期削弱。突然间,这些孩子不再能够奔跑,踢钢琴或爬楼梯,往往依赖于15岁的轮椅。目前,不存在这种情况的治疗。
“现在,我们能够使用CRISPR-CAS9技术访问这些患者的基因突变,”实验和临床研究中心(ECRC)的近距离德布吕克中心联合机构的近世学实验室负责人Simone Spuler教授Helmholtz协会和Charité - Universitätsmedizin柏林的分子医学。“我们在Charité门诊诊所关心2000多名患者肌肉障碍,并迅速认识到新技术的潜力。”研究人员立即开始与一些受影响的家庭合作,现在在期刊上展示了他们的结果江森自控的洞察力。在学习的家庭中,父母健康,不知道他们拥有突变的基因。孩子们都遗传了父母两种疾病突变的副本。
编辑过的人类肌肉干细胞在小鼠体内发育成肌肉纤维
术语 '肌营养不良症'用于指大约50个不同的疾病。“他们都采取了相同的课程,但由于不同基因的突变而有所不同,”筛子解释道。“甚至在基因内,不同的部位也可以突变。”在对所有患者的基因组分析后,研究人员由于它们的特殊形式的疾病而选择了一个家庭:肢体 - 腰带肌营养不良2-D / R3相对常见,迅速进行,并为“遗传剪刀”具有合适的对接部位'接近DNA上的突变。
对于该研究,研究人员从十岁患者中拍摄了肌肉组织样本,隔离干细胞,乘以这些体外,并使用碱性编辑在突变部位替代碱基对。然后它们将编辑的肌肉干细胞注入小鼠肌肉,这可以耐受外国人体细胞。这些乘以啮齿动物,最开发成肌肉纤维。“有了这个,我们能够首次展示它可以用健康的患者取代患病的肌肉细胞,”套管说。在进一步测试之后,修复的干细胞将重新引入患者。
基本编辑 - 一种复杂的技术
碱基编辑是CRISPR-Cas9基因编辑工具的一种更新和高度复杂的变体。然而在“经典”方法中,两条DNA链都被这些分子剪刀剪断,用于碱基编辑的Cas酶仅仅是从一个特定的碱基上剪掉剩余的葡萄糖,然后附着在另一个上,从而在目标位点创建一个不同的碱基。“这个工具的工作原理更像是镊子而不是剪刀,它非常适合进行基因的定点突变,”斯普勒团队的分子生物学家海伦娜·埃斯科巴博士说。“这也是一种更安全的方法,因为不希望发生的变化极其罕见。”在经过基因修复的肌肉干细胞中,我们没有看到任何基因组非预期区域的错误编辑。”Escobar是这项研究的主要作者,也是开发肌肉细胞技术的人。
自体细胞治疗- 它涉及删除患者自己的干细胞在体外编辑它们,然后将它们注射回肌肉——这将不能使那些已经离不开轮椅的患者再次行走。“我们无法修复已经萎缩并被结缔组织取代的肌肉,”斯普勒强调说。而且可以在体外编辑的细胞数量也很有限。然而,这项研究首次证明了一种疗法甚至可以用于治疗一组以前无法治愈的疾病,它可以用于修复小肌肉缺陷,比如手指屈肌缺陷。
靠近治疗的一步
但这只是第一步。“下一个里程碑将是找到一种方法,可以直接进入患者进入患者。一旦在身体内,它会”游泳“一小段时间,编辑所有肌肉干细胞,然后很快又崩溃了。”该团队希望尽快在老鼠模型上进行第一次试验。如果这也能奏效,将来就可以对新生儿进行相应的基因突变检测,并在相对较少的时候开始治疗细胞需要编辑。
那么,具体来说,肌肉萎缩症的体内治疗是什么样子的呢?科学家们已经用病毒载体在动物模型上进行了一段时间的实验。然而,海伦娜·埃斯科瓦尔解释说,因为这些载体在体内停留的时间太长,错误编辑和毒性作用的风险太大了。分子生物学家说:“另一种选择是使用包含编辑器在体内合成工具信息的信使rna分子。”“mRNA在体内分解得非常快,所以治疗酶只能在短时间内保持活跃状态。”如果必要的话,这种治疗可能还会重复进行。“我们还不知道这是否需要一个涉及多个应用程序的治疗周期。”
这种治疗大道意味着,与自体细胞疗法不同,并非每只患者都需要单独治疗。对于每种形式的肌肉治疗,一个“工具”就足以治愈肌肉在重大损害之前萎缩甚至发生了萎缩。但是,现在,这仍然很长的路。















用户评论