科学家们对凝血机制的发现可能会带来新的抗血栓药物
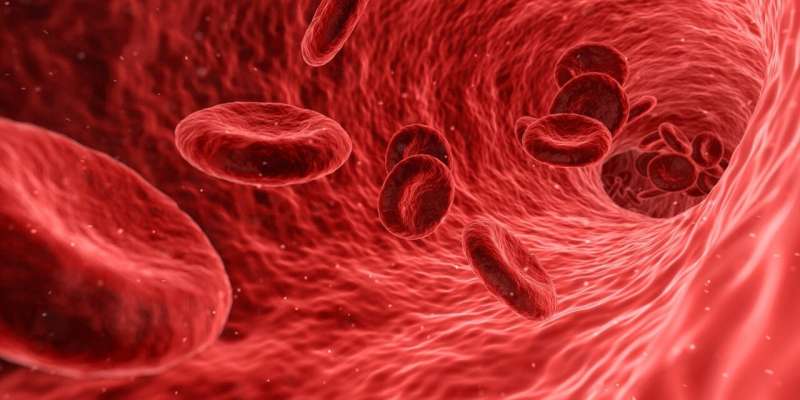
在正常,健康的循环条件下,血管性血友病因子(vWF)保持自身。这种巨大而神秘的糖蛋白在血液中流动,紧紧地团成一团,其反应部位未暴露。但当发生严重出血时,它就会迅速发挥作用,启动凝血过程。
当它正常工作时,vWF可以帮助止血并拯救生命。然而,根据疾病控制和预防中心(CDC)的数据,每年大约有6万到10万美国人死于血栓形成,一种以凝血过多为特征的疾病。血凝块可以引发中风或心脏病发作。
据利哈伊大学生物工程系副教授X. Frank Zhang称,fda只批准了一种针对vWF并治疗血栓或过度凝血障碍的药物Caplacizumab。它通过与vWF结合并阻止它与血小板结合来发挥作用。然而,没有人知道它实现这一目标背后的具体机制。
到目前为止,Zhang和他来自埃默里大学医学院和诺丁汉大学的同事们第一次确定了vWF的特定结构元素,使其能够与血小板结合并启动凝血。研究小组称,这种被称为不连续自抑制模块(AIM)的特定单元是新药开发的主要部位。上周发表在《科学》杂志上的一篇文章描述了这项工作自然通讯,"通过机械展开其不连续的自抑制模块来激活血管性血亲因子"
“AIM模块允许vWF分子在正常循环血液中保持不反应,并在出血时立即激活vWF,”张说。“在我们的研究中,我们发现Caplacizumab通过结合vWF的AIM区域并提高力阈值来机械地去除vWF的自抑制结构,从而为开发靶向于AIM结构的抗血栓药物开辟了新的途径。”
张说,vWF的一个基本特征是,在血液循环的大部分时间里,它对血小板保持不反应。然而,在出血部位,vWF几乎可以立即被激活来实现血小板粘附和血凝块的形成。在这项研究中,研究小组确定了一个位于vWF的A1结构域附近的结构元件AIM,它负责与血小板结合。
“在正常循环的血液中,”张解释说,“AIM包裹A1,防止A1与血小板相互作用。然而,在结合位点,血流动模式的改变导致了足够的水动力来拉伸目标,并将其从A1拉离,使A1抓住血小板到达出血部位。”
张教授从事vWF研究多年,专长于单分子力谱和机械感测,即细胞对机械刺激的反应。他使用一种专门的工具光镊该技术利用聚焦激光束对小至单个分子的物体施加力。
“光镊可以抓取微小的物体,”张解释说。“我们可以抓住vWF,同时施加力来观察蛋白质如何改变形状,看看当存在机械扰动或机械力时,蛋白质是如何被激活的。”
张说,在进行这项研究之前,根据埃默里大学的共同通讯作者李仁浩先前的研究,该团队怀疑他们会发现一种自我抑制模块。
“然而,我们没有想到这个抑制模块在vWF中扮演如此重要的角色,”张说。“它不仅控制血小板相互作用的vWF激活,而且在引发某些类型的血管性血友病中发挥作用,这是一种遗传性出血疾病,影响1%的人类。”














用户评论