新的埃博拉病毒疫苗设计寻求驱动更强的抗体防御
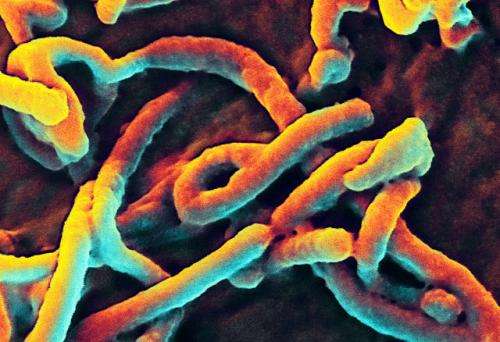
斯克里普斯研究中心(Scripps Research)的科学家公布了一种新的埃博拉病毒疫苗设计,他们说,对于继续威胁全球健康的埃博拉病毒和相关病毒,这种疫苗比标准疫苗方法有几个优势。
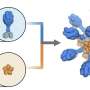
在新设计中,在一篇论文中描述了自然通讯,埃博拉病毒外刺突蛋白的副本,被称为糖蛋白,系在球形载流子的表面上。由此产生的结构类似于感染人类的普通RNA病毒的球形外观,与蛇形的埃博拉病毒截然不同。
科学家们说,这种设计的目的是激发比标准更好的保护性免疫反应疫苗这种方法常常使免疫系统暴露于单个糖蛋白而不是真实的外观病毒颗粒。
在设计疫苗时,研究人员还修改了外部刺突蛋白,使其比在实际埃博拉病毒中发现的正常“野生型”版本更稳定。在小鼠和兔子身上的测试中,他们发现这种稳定的版本比之前埃博拉疫苗中使用的野生型糖蛋白引发的病毒中和抗体更强。
斯克里普斯研究所综合结构和计算生物学副教授、该疫苗的发明者朱江博士说:“在这里,我们对糖蛋白稳定性进行了一步一步的调查,以及它如何影响疫苗诱导抗体的能力。”“最终,我们开发出了一款非常有前景的游戏疫苗设计。"
持续的病毒威胁
埃博拉病毒在非洲各种蝙蝠身上流行,并能传染给人类,导致出血热爆发,死亡率很高。已知最大的一次疫情发生在2013-2016年期间的西非,导致1.1万人死亡。
大约20年前,加拿大研究人员开发了一种针对扎伊尔伊波拉病毒的疫苗,俗称伊波拉病毒。该疫苗后来被授权给一家大型制药公司,名为rVSV-ZEBOV,它使用了一种活病毒——水疱性口炎病毒——经过修饰,加入了埃博拉病毒糖蛋白的基因。
当注射时,rVSV-ZEBOV疫苗会感染细胞并产生糖蛋白副本,引发免疫反应,以防止未来暴露于埃博拉病毒。在上述疾病爆发期间在非洲进行的测试表明,该疫苗效果良好,并于2019年底获得了美国食品和药物管理局(Food and Drug Administration)的批准。然而,这些试验缺乏安慰剂组和其他典型的大规模iii期试验的标准特征。因此,关于真正功效的问题仍然存在。
在开发新的埃博拉病毒疫苗设计时,Zhu和他的团队专注于糖蛋白结构的相对不稳定性,这是疫苗有效性的一个潜在因素。他们详细研究了这种不稳定性的分子来源,并最终提出了一系列极大地稳定糖蛋白的修饰。在小鼠和兔子身上,他们修饰过的糖蛋白对两种不同的埃博拉病毒——马科纳株埃博拉病毒和本迪布焦株埃博拉病毒——引发了更有效的中和抗体反应,并与野生型糖蛋白进行了比较。
该团队的设计还包括特殊的蛋白质片段,这些蛋白质片段可以自组装成球形的“纳米颗粒”,在其表面支持多种糖蛋白。这种基于纳米颗粒的结构将糖蛋白呈现给免疫系统,类似于普通的人类病毒,因此人体已经学会了识别球形颗粒。
朱解释说:“把我们的纳米颗粒想象成你的运动车辆,车顶上有一个架,可以载一辆山地车,还有一个后备箱,可以存放你的衣服、齿轮和食物。”“唯一的区别是,埃博拉病毒峰值出现在你的山地车里,而锁定域和t细胞表位是你后备箱里的东西。”我们称之为多层设计。”
一种新方法
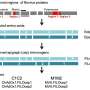
这种纳米颗粒设计与其他纳米颗粒平台截然不同。Zhu解释说,在他的团队的设计中,优化的糖蛋白的遗传密码、纳米颗粒形成单元、锁定域和t细胞表位都包含在一个DNA片段中。在细胞中,这种DNA产生一条可以自我组装的蛋白质链,形成正确的结构,并与其他相同的链结合,形成一个多层的类似病毒的蛋白质球。
朱说:“这种一体化的设计简化了生产过程,降低了疫苗成本。”
他的团队已经使用纳米颗粒平台创造了COVID-19候选疫苗,在动物模型中显示,它可以诱导对SARS-CoV-1和SARS-CoV-2产生强大的抗体应答。它也被证明对变种有效。
对于埃博拉病毒,纳米颗粒疫苗在只使用糖蛋白刺激免疫反应的小鼠和兔子病毒中和试验中显示出了更好的结果。用易于分解的埃博拉野生型糖蛋白接种动物后,有迹象表明一种称为抗体依赖增强的疫苗现象——疫苗不仅能产生病毒中和抗体,而且还能矛盾地增加病毒感染细胞的能力。研究人员发现,他们最好的基于纳米颗粒的设计只会最小程度地引发这些不良抗体。
“埃博拉病毒疫苗领域还有很多东西需要仔细研究,但在这项研究中,我们最终得出了两种基于纳米颗粒的设计,它们似乎非常适合进一步优化和测试,”朱说。
他说,这种疫苗方法可以推广到同一病毒家族的其他成员,比如马尔堡病毒病毒,这也是一个主要威胁。埃博拉病毒和马尔堡病毒都属于丝状病毒的一组,在显微镜下看到的丝状病毒有奇怪的线状形状。
该研究还包括了修饰糖蛋白的原子级晶体结构,这是与Ian Wilson博士的实验室合作完成的,Hansen教授的结构生物学和综合结构和计算生物学系主任。
进一步探索










用户评论