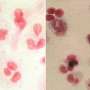
基因疗法为先天缺乏免疫系统的儿童提供了潜在的治愈方法

一组来自加州大学洛杉矶分校和伦敦大奥蒙德街医院的研究人员开发了一种实验性的基因疗法,成功地治疗了50名天生患有罕见致命遗传疾病的儿童中的48名。这种疾病会使他们失去免疫系统。
由腺苷脱氨酶缺乏引起的严重联合免疫缺陷(ADA- scid)是由产生腺苷脱氨酶的ADA基因突变引起的,而腺苷脱氨酶对免疫系统的正常运作至关重要。对于患有这种疾病的儿童来说,即使是像上学或和朋友玩耍这样的日常活动也会导致危险的、危及生命的感染。如果不治疗,ADA-SCID可能在生命的头两年内致命。
研究基因治疗方法包括首先收集一些孩子的造血干细胞它们有可能产生各种类型的血液和免疫细胞。接下来,使用研究团队开发的一种方法,通过改良的慢病毒或“病毒载体”将ADA基因的新拷贝传递到干细胞中。经过修复的细胞随后被送回孩子的身体,在那里它们将产生持续的健康供应免疫细胞能够抵抗感染。
今天发表在新英格兰医学杂志在该研究中,加州大学洛杉矶分校的唐纳德·科恩博士和大奥蒙德街医院(Great Ormond Street Hospital,简称GOSH)的克莱尔·布斯(Claire Booth)博士报告了2012年至2017年期间在大奥蒙德街医院、加州大学洛杉矶分校美泰儿童医院和美国国立卫生研究院在临床试验中接受研究性慢病毒基因疗法治疗的儿童两到三年的结果。
在这三者之间临床试验Kohn是一位微生物学、免疫学和分子遗传学的杰出教授,也是加州大学洛杉矶分校再生医学和干细胞研究Eli and Edythe Broad中心的成员。“所有患者都活得好好的,其中95%以上的患者,这种疗法似乎已经纠正了他们潜在的免疫系统问题。”
患者中无并发症或治疗限制事件报告。大多数不良事件为轻度或中度,并被认为与实验基因治疗准备过程中的常规操作或免疫系统重建影响有关。
Kohn说:“在50个病例中,除了两个之外,所有的治疗都是成功的,这两个孩子都能够恢复到目前的标准护理疗法和治疗,其中一个最终接受了骨髓移植。”Kohn已经致力于开发针对ADA-SCID和其他血液疾病的基因疗法35年了。
研究人员说,这种一次性的基因疗法可能会产生终生的效果,对于患有ADA- scid的儿童来说,这是一种受欢迎的潜在的新治疗选择,否则他们必须每周注射一两次ADA酶,直到找到匹配的骨髓捐赠者(通常是亲近的家庭成员)。如果没有供体,患者就需要终生注射,以及抗生素、抗真菌药物和每月注射含有抗感染抗体的免疫球蛋白。这些治疗费用昂贵,因此许多国家的患者无法获得。
“如果在未来获得批准,这种治疗可能成为ADA-SCID的标准治疗方法,并可能成为许多其他遗传疾病的标准治疗方法,这样就不需要为a寻找匹配的供体骨髓移植以及通常与这种治疗相关的毒副作用,”布思说,他是伦敦大医院儿童免疫学和基因治疗方面的顾问。
慢病毒基因疗法的好处
在合作之前,布斯和科恩分别工作了多年成功的基因疗法ADA-SCID使用了由逆转录病毒制成的病毒载体。然而,逆转录病毒载体只能进入细胞核进行传递基因在细胞分裂的过程中,接受基因负载的细胞数量受到限制,从而限制了治疗的潜在疗效。
此外,虽然Kohn和Booth在他们的ADA-SCID试验中都没有观察到严重的并发症,但其他早期测试逆转录病毒载体基因疗法的研究确实报告了一些严重的副作用,包括在一些患者中发生白血病。
2008年,布斯和科恩开始与伦敦大学学院的鲍比·加斯帕和阿德里安·思拉舍教授合作,利用另一种称为慢病毒的病毒,开发一种改进的病毒载体。这种病毒可以进入非分裂细胞的细胞核,当被用作载体时,有可能使基因疗法更安全、更有效。ADA-SCID患者在2012年开始接受新的基因治疗;第二年,加州大学洛杉矶分校和美国国立卫生研究院提供了实验性治疗。
Thrasher是该研究的资深作者,同时也是伦敦奥古斯医院的儿科免疫学教授,他说:“目前,全世界有200多名患有各种遗传疾病的患者已经接受了实验性慢病毒基因疗法的治疗,将基因疗法应用于ADA-SCID是另一项重大的科学进步。”
在加州大学洛杉矶分校的研究中,有10名儿童使用了冷冻的校正干细胞制剂进行治疗。这些儿童与使用未冷冻细胞的儿童经历了类似的结果。冻结的方法可能行得通孩子们与ADA-SCID合作干细胞在当地收集,然后在其他地方的生产设施运输和加工,再运回附近的专科医院,这样患者和他们的家人就不需要长途跋涉到专科中心。