避免童年牙齿腐烂的温和策略
高碳水化合物饮食和糟糕的口腔卫生可能会让儿童患上幼儿龋齿(ECC),这是一种严重的龋齿形式,会对他们的口腔和整体健康产生持久影响。
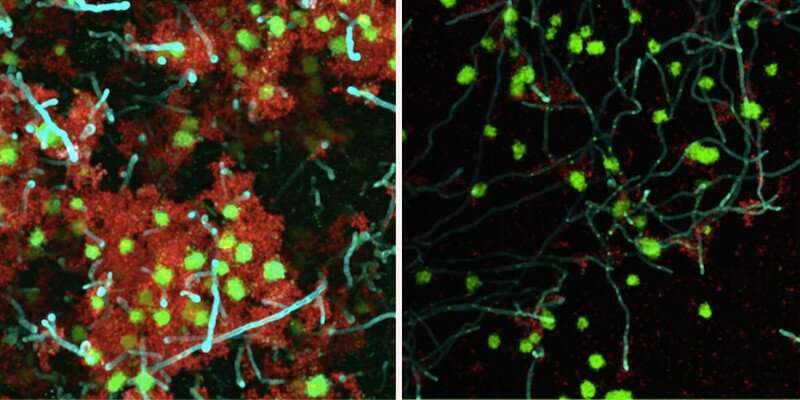
几年前,宾夕法尼亚大学牙科医学院的科学家们发现,导致ECC的牙菌斑由一种细菌物种——变形链球菌和一种真菌——白色念珠菌组成。这两者形成了一种粘着的共生关系,科学上称之为生物膜,这变得非常毒性,难以取代齿面。
现在,该小组的一项新研究提供了一种策略,通过针对使ECC斑块如此棘手的酵母-细菌相互作用来破坏这种生物膜。与某些人相比目前的治疗ECC使用的抗菌剂可能产生脱靶效应,可能损害健康组织,这种治疗使用一种特定于存在于微生物之间的键的酶。
“我们认为这可能是一种处理ECCs问题的新方法,ECCs会干预细菌和酵母之间的协同作用,”宾夕法尼亚牙科医学的助理教授Geelsu Hwang说,他是发表在该杂志上的这项研究的资深作者mBio。“这为我们提供了破坏这种毒性生物膜的另一种工具。”
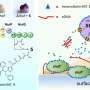
这项工作建立在2017年Hwang和他的同事,包括宾夕法尼亚牙科医学的Hyun (Michel) Koo的一篇论文的基础上,他们发现念珠菌细胞壁上的甘露聚糖分子与变异链球菌分泌的一种酶紧密结合,即糖基转移酶(Gftb)。除了促进跨界结合,Gftb还通过在糖存在的情况下制造称为葡聚糖的胶状聚合物来促进牙齿生物膜的顽强性。
虽然某些ECC病例被直接杀死微生物的药物,但可能减少口腔中病原体的数量,这并不总是有效地分解生物膜,并且可以对“良好”的微生物有脱靶效应。口腔中的软组织。
Hwang和他的同事们想尝试一种不同的方法,直接瞄准酵母和细菌之间的潜在相互作用,并选择瞄准念珠菌细胞表面的甘露聚糖作为接触点。
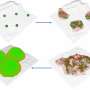
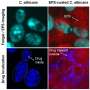
他们使用三种不同的甘露聚糖降解酶,将每种酶分别应用于人类唾液培养基中生长在牙齿表面的生物膜上,并让其停留5分钟。治疗后,他们注意到总的生物膜体积减小了。利用高倍显微镜,他们还观察到生物膜的厚度以及细菌和酵母之间的相互作用急剧减少。当接触到这些酶时,周围介质的pH值会更高,这表明环境没有那么酸性,因此不利于蛀牙。
他们还使用一种类似于刷牙的施加压力的设备,测量了治疗后打破生物膜的容易程度。
“生物膜结构更脆弱后酶治疗,”黄说。“我们可以看到,生物膜更容易去除。”
为了确认他们的方法的机制——甘露聚糖降解酶正在削弱酵母和细菌之间的结合——该团队使用原子力显微镜来测量念珠菌和Gftb之间的结合。他们发现,这种疗法将这种约束力降低了15倍。
最后,他们想要了解这些酶使用在口腔,尤其是儿童将成为患者的目标群体。
他们将这种酶应用于培养的人类牙龈细胞,发现即使使用浓缩形式的酶,也没有有害影响。此外,他们还观察到,这种疗法并没有杀死细菌或酵母,这表明,即使微生物发生突变,从而对其他类型的疗法产生耐药性,这种疗法也可能有效。
研究人员将涂抹时间保持在相对较短的5分钟,尽管他们希望能在更短的时间内看到活动,比如建议的刷牙两分钟。黄说,他们可能会考虑一种添加了这些酶的非酒精基漱口水,可以用于儿童预防措施针对ECC。
研究人员希望通过后续研究继续探索这种可能性,包括在动物模型中测试这些酶。随着更多的成功,他们打算增加另一种工具,以对抗ECC的公共卫生威胁。









用户评论