基因表达调节剂的蛋白质改性可以赋予炎症神经保护剂
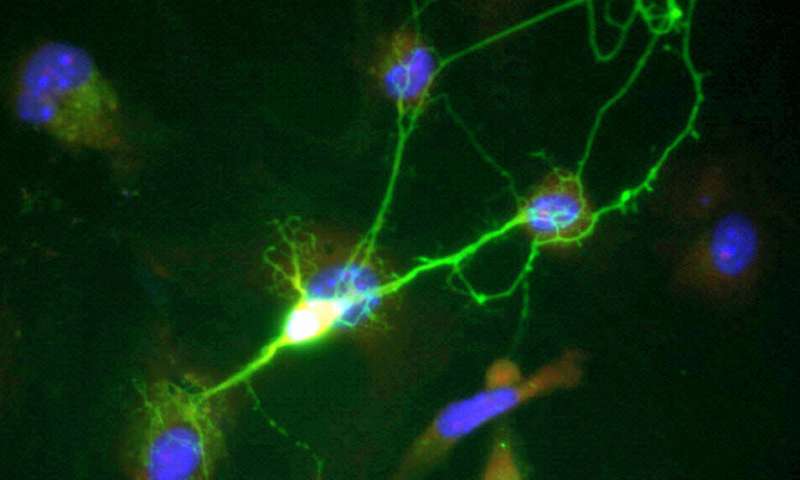
芬兰东部大学的研究人员发现了蛋白质修饰的潜在神经保护作用,其可能是早期阿尔茨海默病的治疗靶标。新的研究调查了MECP2,基因表达调节因子在脑细胞中的阿尔茨海默病相关过程中的作用。该研究发现,随着阿尔茨海默病的进展,大脑的特定氨基酸下的MECP2蛋白的磷酸化降低。在炎症刺激上消除了培养的小鼠神经元在培养的小鼠神经元中的这种磷酸化增强了它们的活力,并增加了重要基因在神经元的维护和保护中的表达。在研究中获得的结果称为MECP2的修饰作为开发针对AD和其他神经变性疾病的特异性疗法的潜在目标。该研究最近发表在细胞杂志。
阿尔茨海默病是最常见的痴呆形式,患有全球疾病的40多万人。目前没有治疗疾病的有效预防或治疗。在阿尔茨海默氏病的严重症状之前,如记忆损失和混乱发生,神经元之间的连接丢失,神经元在大脑中染色。神经元不是唯一有助于阿尔茨海默病进展的细胞类型。已显示微胶质细胞,脑的免疫细胞,有助于神经元损伤和损失。虽然轻度激活小胶质细胞可以通过去除来保护神经元有害物质和细胞碎片,它们的慢性活化会导致神经毒性因子的分泌和健康神经元的吞噬。
“MECP2磷酸化的功能几乎完全在神经元中研究。显然,小胶鸡涉及许多人的发病机制神经退行性疾病,我们选择专注于微胶质细胞和微胶囊的神经元的共同培养。为了另外模拟微胶质细胞的激活,我们通过用不同的化合物治疗诱导炎症,“早期研究员Rebekka Wittrahm说。
在来自阿尔茨海默病的不同阶段的验尸脑样本中,该研究发现,在阿尔茨海默病的早期阶段的氨基酸丝氨酸423,MECP2蛋白的磷酸化降低。因此,问题在丝氨酸423在丝氨酸423中的MECP2不磷酸化,当在培养的小胶质细胞或神经元微胶质植物共培养物中表达时,会改变细胞过程。为了研究该问题,在不同的细胞培养模型中表达野生型MECP2和丝氨酸423以防止磷酸化的变型。在微胶质细胞中,研究人员发现,野生型MECP2的过度表达导致颗粒的吞噬摄取降低。在激活微胶质细胞后,野生型MeCP2的表达增强了它们对刺激的炎症反应。对于大多数分析的参数,MECP2丝氨酸423的阻断磷酸化与野生型蛋白相比没有导致主要变化。
与来自小胶质神经胶质的结果相比,蛋白质的表达神经元用小胶质细胞共培养野生型和突变的MECP2之间的几个差异。RNA测序分析显示,在微胶质激活时阻断丝氨酸423磷酸化增加了几种已知有助于维持和保护细胞的神经元基因的表达。“需要更广泛的实验,但可以想到它在丝氨酸423处的MECP2的去磷酸化可能是一种机制细胞在阿尔茨海默病的早期阶段介导神经保护,“Rebekka Wittrahm考虑。
总之,本研究结果表明MECP2丝氨酸423是必不可少的磷酸化在神经炎症中调节神经元基因表达中可能发挥作用的遗址。该研究称之为MECP2的修改网站是开发针对阿尔茨海默氏症的特定疗法的潜在目标的想法疾病和其他未来的神经退行性疾病。










用户评论