团队报告基因编辑IPS细胞如何导致通用癌症免疫治疗产品
癌症免疫治疗使这些消息成为对某些癌症的惊人的效果。然而,目前的临床疗法主要使用患者自己的细胞,限制了可以获得这种治疗的患者的数量。Cira教授Shin Kaneko正在开发IPS细胞技术,这些技术将为所有患者提供癌症免疫治疗。在一项新的研究中,他的研究团队报告了基因编辑IPS细胞如何导致普及癌症免疫疗法,这些免疫疗法不依赖于患者的细胞。
癌症免疫治疗描述了一种使用患者自己的免疫系统来战斗的一系列疗法癌症。在采用细胞疗法中,免疫细胞在肿瘤中发现被除去,加工以增强它们的抗癌效力,并返回患者。
“对收养的细胞疗法有很多兴奋。然而,处理需要时间,患者的病情恶化。加上,根据患者的病症,有时不能使用细胞,”kaneko解释说。
细胞Kaneko重点是T细胞,具有最强的抗癌反应。来自第三方捐赠者的T细胞是一种替代方案,但他们带来了自己的风险。
“癌症免疫疗法的理想T细胞产物不仅需要对癌症有效,”持续的Kaneko“需要避免宿主的免疫系统和移植物与宿主疾病。”
移植物与宿主病和宿主与移植反应是器官移植和细胞疗法需要患者捐赠者匹配的原因。尽管移植到患者的移植物的良好意图,但如果没有完成匹配,那么供体的免疫细胞或患者的免疫系统可以引发剧烈的反应,这可能比疾病本身更危险。
免疫细胞通过其受体响应异细胞表达的蛋白质。这些蛋白质中最重要的是人白细胞抗原(HLA),但还有其他蛋白质。
“需要抑制三种类型的免疫细胞,以使移植物存活。CD8 T细胞导致最强,最危险的反应,但也必须考虑CD4 T细胞和NK细胞,”Kaneko说。
不同的细胞类型复杂化匹配,这就是为什么患者自己的细胞用于采用细胞免疫检查,即使它们被患者的病症受到损害。
几个组探索了基因编辑以消除来自接枝T细胞的HLA和其他免疫激活蛋白。然而,正如该研究的第一作者所解释的那样,这种解决方案可能会损害T细胞。
“当它们与癌细胞接触时,Heathy T细胞膨胀。然而,多轮基因编辑削弱了这种膨胀能力。它还使T细胞变得疲惫不堪,”他说。
疲惫是癌症中的常见问题,表明可以靶向癌症但不能杀死它的T细胞。
iPS细胞可以为这些问题提供一个解决方案。iPS细胞具有无限的扩张潜力,可以分化成任何类型的细胞,包括用于过继细胞免疫治疗的T细胞。重要的是,它们的扩增和分化潜能都不受多轮基因编辑的影响。
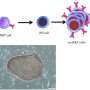
因此,研究人员探讨了哪些基因为了编辑,选择B2M,用于CD8 T细胞,CITTA用于CD4 T细胞和NK细胞的特定类型的HLA(HLA-e)。先前已知所有这些基因调节相应的免疫细胞的活化。此外,它们敲出了PVR基因,进一步降低了NK活性。然后将编辑的IPS细胞分化为T细胞(IPS-T细胞),发现其未刺激的情况下具有良好的抗癌作用免疫细胞。
嵌合抗原受体(汽车)T细胞疗法是最有效的癌症免疫治疗。汽车是一种合成受体,极大地提高了T细胞的发现和杀死癌细胞的能力。临床中的当前汽车治疗使用患者自己的T细胞,其具有上述相同的缺点。Kaneko Lab一直将汽车技术整合到IPS-T细胞中,并确认基因编辑并未损害汽车效果。
因此,科学家们将CAR加入iPS-T细胞中,并将细胞注射到患有白血病的小鼠体内。CAR - iPS-T细胞也可以通过基因编辑来躲避免疫系统,其抗癌效果要比那些没有这种基因编辑的细胞强得多。
“我们的实验发现,人源化小鼠中的CD4和CD8 T细胞被野生型汽车IPS-T细胞刺激。如果我们首先编辑该基因,那不是这样的,”王。
编辑的IPS细胞显示出可用于任何可用于任何癌症患者的T细胞的通用来源。
“我们的目标是开发一个普遍的免疫治疗产品。将我们的IPS细胞与汽车技术结合起来将使我们将来会准备现成的免疫治疗,”Kaneko说。
进一步探索









用户评论