14-3-3sigma基因作为一个肿瘤抑制肠道癌症
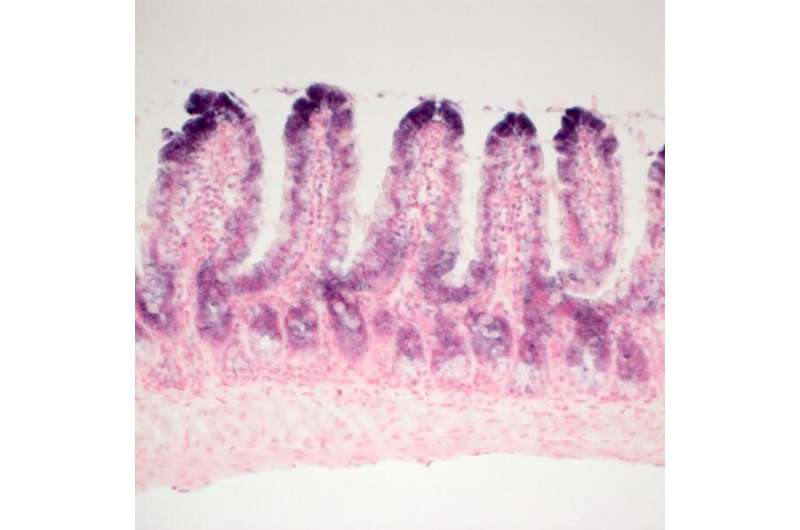
LMU研究人员已经确定了14-3-3sigma基因作为一种重要的抑制胃肠道的致癌作用。
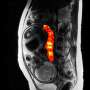
肠道癌症,也被称为结肠直肠癌,是全球最普遍形式的恶性肿瘤之一。如果及早发现,可以通过手术切除肿瘤。然而,随着肿瘤生长的发展,细胞可能会逃离原发肿瘤,然后在其他器官建立转移性肿瘤。一旦这些卫星肿瘤形成,存活率显著下降。形成最初的肿瘤可以通过突变引发的吗基因。一起博士后马库斯冬季和Matja Rokavec,海科Hermeking教授LMU病理学研究所的已经发现一种叫做14-3-3sigma函数作为一个肿瘤抑制胃肠道癌症。以鼠标为实验模型,研究小组证明14-3-3sigma基因的失活增强胃肠道癌症的进展,从而缩短小鼠的寿命。
在早期与结肠癌细胞系,Hermeking和他的同事们表明,蛋白质被称为p53,起着核心作用的抑制多种肿瘤,激活14-3-3sigma基因,其抑制通过细胞周期蛋白产品。这种抑制细胞分裂使细胞更多的时间来修复不定或环境引起的DNA损伤,因此减少细胞增殖失控的风险。p53突变灭活中发现超过一半的肿瘤。”,但尚不清楚是否14-3-3sigma基因本身起着重要的作用在抑制肿瘤发生肠,“Hermeking说。
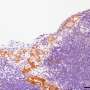
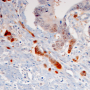
在德国癌症研究基金会资助的一个项目(德意志Krebshilfe),他的团队开始澄清这个问题通过分析在几个成千上万的肿瘤样本的基因表达模式与结直肠癌患者。数据显示,14-3-3sigma确实的表达显著下调这些肿瘤。此外,在转移性肿瘤效果尤为明显,基因的表达水平与癌症恶化的程度呈负相关。此外,14-3-3sigma基因的表达水平较低的病人被发现有一个糟糕的预后比那些高表达和发现是独立的肿瘤是否还包含一个灭活p53基因的突变。
进一步探索14-3-3sigma在肠道癌形成的意义,LMU研究者专门灭活基因在临床前肠的小鼠模型癌症。损失的基因的功能被发现刺激肿瘤的形成和生长胃肠道,并最终降低生存时间。后来的研究表明,在缺乏14-3-3sigma基因信号通路调节的转录因子,参与转移的形成是有选择性地诱导。有趣的是,14-3-3sigma已知蛋白质绑定和负调控这些转录因子。“综上所述,我们的结果表明,14-3-3sigma不仅是一个多目标控制的基因p53以及调节其肿瘤抑制功能,还有自己在胃肠道肿瘤抑制功能,“Hermeking说。
作者的研究表明,检测14-3-3sigma基因的表达减少结肠切除原发性癌可以作为患者人群的预后指标。“此外,触发的信号通路在其失活是潜在的治疗干预的目标,“Hermeking补充道。
进一步探索