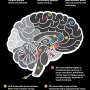
有一种新的阿尔茨海默病药物,那么问题是什么呢?一位医生解释道。

在对600多万阿尔茨海默病患者的潜在治疗方法进行了多年令人失望的研究后,美国食品和药物管理局(fda)最近批准了一种名为aducanumab的新药,该药物肯定会引起人们的极大兴趣。
然而,这种药物遵循了一种不同寻常的监管路径,并没有说服一个关键的顾问小组相信它是有效的。
内科医生、约翰霍普金斯大学布隆伯格公共卫生学院流行病学和医学教授G. Caleb Alexander博士曾是该委员会的成员,他在接受《巴尔的摩太阳报》采访时谈到了这种新药。
那么,为什么人们对这种药议论纷纷呢?
阿尔茨海默氏症是一种以记忆丧失、思维混乱和最终死亡为特征的痴呆症,目前还无法治愈。自2003年以来,没有一种新药获得批准。亚历山大说,人们需要新的治疗方法。
倡导团体一直在推动批准这种疗法,因为它可以延缓症状,但不能阻止疾病的发展。
阿尔茨海默氏症协会首席执行官Harry Johns称aducanumab的批准是阿尔茨海默氏症患者及其家人的胜利,并表示这将给患者“更多时间更好地生活”。但他说,这项批准不是终点,而是“让科学家和公司重新振作起来,与这种疾病的祸害作斗争”。
研究表明了什么?
总部位于马萨诸塞州坎布里奇的Biogen Inc.生物科技公司日本制药公司卫材公司(Eisai Co.)开发了一种名为Aduhelm的药物,并在早期阿尔茨海默病患者身上进行了三次大型临床试验。
在没有显示出任何益处后,研究于2019年停止,但在这些公司重新审视了其中一项研究的数据后,研究恢复了。他们发现它减少了大脑中一种叫做β -淀粉样蛋白的粘性蛋白质。
亚历山大说,当这种蛋白质积累时,斑块是导致患者脑细胞死亡和病情恶化的主要嫌疑人。
这是第一种被证明可以减少斑块的药物。
Biogen首席执行官Michel Vounatsos在一份声明中说:“我们相信,这种一流的药物将改变阿尔茨海默病患者的治疗方式,并在未来几年激发持续的创新。”
这种药物是如何获得FDA批准的?
FDA对这种药物进行了加速批准,这是针对严重或危及生命的疾病的治疗程序。根据监管机构的说法,这是基于它将为患者带来益处的合理可能性,监管机构要求制药公司继续研究这种药物数年。
“目前可用的治疗方法只治疗疾病的症状;FDA药物评估和研究中心主任Patrizia Cavazzoni博士在一份声明中说:“这种治疗方案是第一种针对并影响阿尔茨海默病潜在疾病过程的治疗方法。”
她说,批准将更快地为患者带来一种疗法,同时“刺激更多的研究和创新”。
这个过程有什么不寻常之处?
亚历山大说,有几件事是不寻常的,从在试验失败后重新启用这种药物,到FDA根据一项研究的数据批准这种药物,他称之为“模糊”的证据表明它可以减轻症状。
FDA自己的顾问团去年秋天建议反对批准。
他说:“在真正意义上,有大量的需求没有得到满足,对于可能亲身经历这种疾病的患者及其亲人来说,这是一种明显的紧迫感。”
“但该产品是否能起作用存在着巨大的不确定性,”他说。“最终,FDA决定批准该产品,不是基于其在改善阿尔茨海默氏症症状方面的证明有效性,而是基于其降低β -淀粉样蛋白水平的能力。”
现在发生了什么?
这些公司可以开始运送这种药物。通常情况下,保险公司会为获得fda批准的治疗方案买单。这些公司将这种通过输液进行的治疗定价为每年5.6万美元。
该试验只对早期阿尔茨海默氏症患者进行了药物测试,但FDA对标签没有限制,让医生决定给谁开处方。保险公司尚未表示,他们将承担所有患者的费用,以及是否需要在最初或每隔一段时间进行脑成像以显示斑块水平。
亚历山大说,医生和病人将不得不讨论药物它的潜在好处和副作用,包括脑肿胀、头痛和思维混乱。
他说:“患者和临床医生必须共同应对。”
©2021巴尔的摩太阳报。由论坛内容代理有限责任公司分发。