“坏脂肪”抑制杀伤T细胞攻击癌症
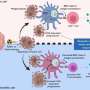
为了让癌症生长和扩散,它必须躲避我们的免疫细胞,特别是专门的“杀手”T细胞的检测。由Susan Kaech教授领导的索尔克大学的研究人员发现,肿瘤内部的环境(肿瘤微环境)含有大量的氧化脂肪分子,当这些分子被杀伤性T细胞吸收时,会抑制它们杀死癌细胞的能力。在一个恶性循环中,那些需要能量的T细胞增加了细胞脂肪转运体CD36的水平,不幸的是,这使它们充满了更多的氧化脂肪,进一步削弱了它们的抗肿瘤功能。
这一发现发表在免疫力2021年6月7日,他提出了通过减少氧化应激来保护免疫系统对抗癌症能力的新途径脂质杀伤T细胞的损伤确定导致免疫抑制的这些因素肿瘤微环境可以导致新的癌症免疫疗法的发展。
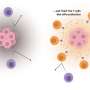
“我们知道肿瘤是一个代谢不利的环境健康的细胞,但要说明是哪一个代谢过程Salk's NOMIS免疫生物学和微生物发病机制中心的资深作者和主任Kaech说:“这些细胞是如何改变的,这如何抑制免疫细胞的功能是癌症研究的一个重要领域,正受到很多关注。”“我们的发现揭示了一种新的肿瘤免疫抑制模式,涉及通过细胞脂肪转运体CD36向T细胞输入氧化脂肪(又称脂质),从而局部损害其抗肿瘤功能。”
新兴的癌症免疫代谢领域研究肿瘤内免疫细胞代谢如何被重新编程,并由营养可利用性的改变驱动。虽然科学家们知道肿瘤会积累脂肪,而且这种积累与免疫功能障碍有关,但这种关系的细节还不清楚。
研究小组与加州大学圣地亚哥分校的约瑟夫·威兹图姆实验室和索尔克质谱中心的安东尼奥·平托合作,确定肿瘤中含有几种脂质含量升高,尤其是氧化脂质,这些脂质通常存在于氧化低密度脂蛋白(ldl)中,通常被认为是“坏”脂肪。然后,他们观察了杀伤T细胞对肿瘤中氧化ldl的反应,发现杀伤T细胞适应了氧化ldl肿瘤微环境通过增加它们表面的CD36和摄入大量的氧化脂质。他们与耶鲁大学Brinda Emu的实验室合作,发现这一过程起到了催化剂的作用,促使杀伤性T细胞内部产生更多的脂质氧化,最终抑制了它们的防御。
接下来,研究小组采用了各种方法来研究CD36如何损害杀伤T细胞的功能。他们在T细胞上建立了缺乏CD36的小鼠模型,并用抗体阻断CD36。他们证实CD36通过增加氧化脂质输入来促进肿瘤中的T细胞功能障碍,这在T细胞内引起更大的脂质氧化和损伤,并触发应激反应蛋白p38的激活。
“我们发现,当T细胞受到氧化脂质的‘压力’时,它们会关闭抗肿瘤功能,”索尔克大学博士后、该论文的第一作者许世豪说。
该团队还发现了新的治疗机会,通过抗体疗法阻断CD36或过表达谷胱甘肽过氧化物酶4 (GPX4,一种清除细胞中氧化脂质的关键分子)的免疫疗法,减少脂质氧化并恢复肿瘤中杀伤T细胞的功能。
重要的是,脂质氧化不仅仅发生在T细胞中;它也发生在肿瘤细胞中,过多会导致细胞死亡。事实上,在癌症研究中,将肿瘤细胞中的脂质氧化提高到致死水平是一件令人兴奋的事情,但Kaech和她的团队敦促人们保持谨慎。
“现在我们已经发现了T细胞对脂质氧化应激的脆弱性,我们可能需要找到更多选择性的方法来诱导肿瘤细胞中的脂质氧化,而不是T细胞中的脂质氧化,”Salk大学NOMIS主席Kaech说。“否则,我们可能会破坏抗肿瘤的T细胞细胞在这个过程中,我们的工作展示了如何做到这一点的一些有趣的可能性。”
进一步探索