乳腺癌干细胞可能利用小动脉微位为转移做准备
今年将有超过4.3万名美国女性死于乳腺癌。大多数死亡发生在癌症扩散到其他器官之后,这一过程被称为转移。这至少包括五个主要步骤。早期的两个步骤是侵入基底膜和细胞迁移,然后癌细胞穿过壁进入血管或淋巴管开始它的旅程。
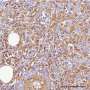
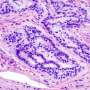
通过检查雌激素受体阳性乳腺癌来自伯明翰阿拉巴马大学的外科副教授、医学博士任斌(Bin Ren)从女性的组织中,首次发现了迄今为止未被注意到的乳房位置的证据癌症干细胞在肿瘤微环境中细胞迁移阶段。癌症干细胞似乎聚集在肿瘤小动脉附近,小动脉是位于毛细血管之前的一个小分支。
Ren将其称为小动脉生态位,他说这可能是一个重要的肿瘤血管微环境,为癌细胞转移做好准备,不仅在乳腺癌中,而且在其他高度血管生成的癌症中,如胶质母细胞瘤、肺癌、恶性黑色素瘤和胰腺神经内分泌癌中也是如此。
乳腺癌干细胞是癌细胞的一个亚群,在转移、生长和耐药性方面最具侵略性。
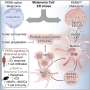
Ren的研究发表在杂志上通信生物学,研究人员发现了乳腺癌干细胞和小动脉内皮细胞之间的交叉对话的证据,使用溶血磷脂酸/蛋白激酶D,或LPA/PKD-1信号通路。通过使用人类乳腺癌组织、小鼠乳腺癌模型和来自基因工程小鼠和细胞培养的血管内皮细胞,观察到这一信号通路促进癌症干细胞特征和小动脉生态位的潜在发展。
根据他们的发现,研究人员提出了一个机械模型。双向作用,通过LPA/PKD-1信号通路,促进内皮细胞的小动脉分化肿瘤微环境癌症干细胞的自我更新和乳腺癌的进展和转移,可能是通过CD36转录的差异调节。
“我们认为这个利基是重要的,它可能存在于其他癌症中,并有丰富的新肿瘤生长血管任说。“这些研究表明,LPA/PKD-1信号通路可能在肿瘤进展中发挥重要作用,并通过培养小动脉生态位的发育来增强癌症干细胞的自我更新,直接促进肿瘤干细胞的干性特征,从而扩散到其他器官,如肺部癌症细胞.靶向LPA/PKD-1 CD36信号通路通过破坏小动脉生态位和有效消除癌症干细胞,可能具有抑制肿瘤进展和转移的治疗潜力。”
进一步探索