糖尿病:饱腹机制研究产生新知识
糖尿病是一种血糖水平长时间保持过高的疾病,长期来看会导致健康并发症。2型糖尿病(T2D)占病例的90%。患者通常肥胖或超重,其危险因素包括久坐不动的生活方式和不平衡的饮食。
为了加深对这种疾病的了解,来自Inserm (Université de Lille)和里尔大学医院里尔神经科学和认知实验室的一组研究人员多年来一直在研究瘦素的作用,瘦素是一种参与食欲控制的激素,它向大脑发送饱腹感信号。在该杂志上发表的一项新研究中自然的新陈代谢,除了进一步的科学认识饱腹的机制,科学家们开发了一种新的小鼠模型这对这一领域的未来研究很有帮助。
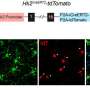
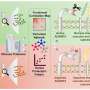
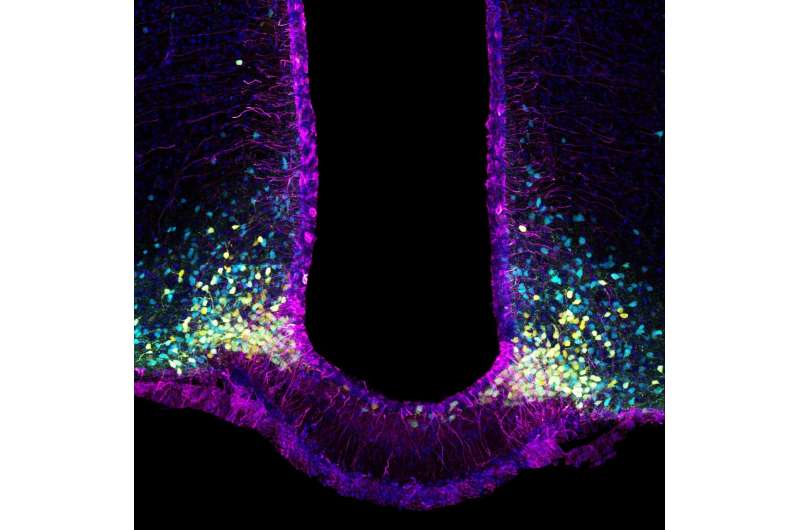
瘦素是一种满足感或食欲抑制激素,由脂肪组织分泌,其分泌水平与身体脂肪储备成正比,通过控制饱腹感来调节食欲。它通过坦尼细胞进入大脑,坦尼细胞附着在LepR受体上。因此,长形细胞是瘦素进入大脑的通道,帮助瘦素穿过血脑屏障并将饱腹感信息传递给神经元。
先前的研究表明,肥胖或超重的人的这种转运功能会受损。这在一定程度上解释了他们的食欲调节功能失调,因为关于饱腹感的信息更难到达大脑。在他们的新研究中,研究人员仔细研究了这种转运机制,更精确地研究了LepR受体所起的作用。
饱腹感激素受体在葡萄糖管理中的关键作用
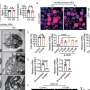
在小鼠模型中,研究人员移除了位于长形细胞表面的LepR受体。三个月后,老鼠的脂肪量显著增加(在此期间增加了一倍),肌肉量也减少了(减少了一半以上)。体重增加的总量只是相当温和的。科学家们还在注射葡萄糖后定期测量动物的血糖水平。
他们发现,为了将血糖维持在正常水平(0.70到1.10 g/L之间),小鼠在实验的前四周分泌了更多的胰岛素。在移除受体3个月后,它们从胰腺分泌胰岛素的能力似乎耗尽了。
因此,去除LepR受体并破坏瘦素向大脑的运输,导致小鼠最初发展为糖尿病前期状态。当身体为了控制血糖而释放出比平时更多的胰岛素时,就会发生这种情况。然后,在较长时间内,小鼠变得无法分泌胰岛素,因此无法控制他们的血糖水平.因此,这些数据表明,瘦素通过LepR受体传输到大脑的受损在2型糖尿病的发展中起着作用。
在他们研究的最后一部分,科学家们将瘦素重新引入大脑,并观察到其胰腺功能的立即恢复——促进作用——特别是胰腺分泌胰岛素以调节血糖的能力。老鼠很快恢复了健康的新陈代谢。
因此,这项研究阐明了大脑在2型糖尿病中的作用,也有助于进一步研究这种此前不被认为涉及中枢神经系统的疾病。
“我们发现,大脑对瘦素的感知对于能量稳态和血糖的管理至关重要。我们还表明,阻止瘦素运输到大脑会损害控制胰腺胰岛素分泌的神经元的功能,”Inserm的研究主任文森特Prévot总结道,他是该研究的最后一位作者。