用于潜在阿尔茨海默病治疗的基因组编辑策略
由香港科技大学(HKUST)科学家领导的一个国际研究团队,利用全脑基因组编辑技术开发了一种新策略,可以在转基因AD小鼠模型中减少阿尔茨海默病(AD)的病理。这种先进的技术为AD患者提供了巨大的潜力,可以转化为一种新的长效治疗方法。
仅在中国,估计就有超过50万名AD家族性阿尔茨海默病(FAD)患者,这是一种与家族史高度相关的先天性AD。虽然FAD有明确的遗传原因,并且可以在认知问题发生之前诊断出来,但事实并非如此有效的治疗目前尚不存在。
利用基因组编辑技术作为由遗传突变引起的疾病(如FAD)的治疗策略,具有巨大的潜力。它尤其适用于在症状出现之前纠正致病基因突变,因此被认为是“一劳永逸”的治疗方法,因为它的效果可以持续一生。然而,有几个障碍阻止了它临床开发还有应用——最明显的是缺乏一种有效、高效和非侵入性的方法来将基因组编辑剂送入大脑。此外,现有的基因组编辑技术无法在整个大脑中产生有益的结果。
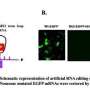
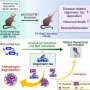
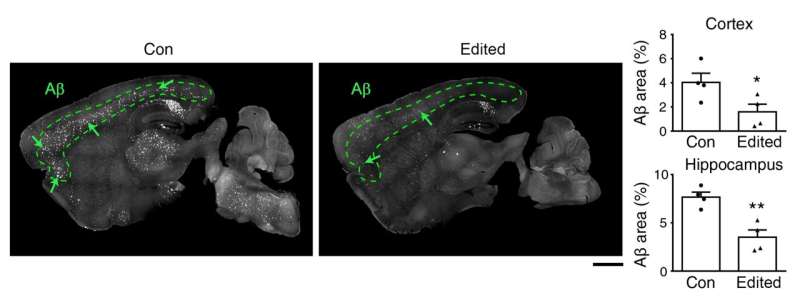
最近,科大负责研究及发展的副校长叶秀娴教授带领的团队,研发了一套新的基因编辑系统,不仅能跨越血脑屏障,还能将优化的基因编辑工具传送至整个大脑。使用一种新设计的基因组编辑传递载体,这种策略通过单一的非侵入性静脉注射实现了高效的全脑基因组编辑。这有效地破坏了AD小鼠模型中fad引起的突变,并改善了整个大脑的AD病理,为疾病的新型治疗发展铺平了道路。
与此同时,研究团队还在小鼠模型中发现,淀粉样蛋白(一种被认为驱动AD神经退行性变的蛋白质)的水平在治疗后6个月(约为正常寿命的1/3)保持在较低水平,这表明这种单次基因编辑策略具有持久的效果。更重要的是,到目前为止还没有在小鼠身上检测到副作用。
身为香港科技大学晨兴生命科学教授及分子神经科学国家重点实验室主任的叶教授说:“这是首个有效的全脑基因组编辑,可在整个大脑缓解阿尔茨海默氏症的病理,真是一个令人兴奋的发展。”“我们的工作是使用基因组编辑治疗遗传性疾病的一个重要里程碑大脑疾病,并有助于发展针对遗传形式的神经退行性疾病的精准医学。”
这项研究是共同努力科大科学家之间的交流;加州理工学院;以及中国科学院深圳先进技术研究院。研究结果最近发表在自然生物医学工程.
进一步探索