辉瑞公司寻求COVID-19 FDA好的疫苗剂量升压

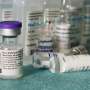
辉瑞公司正寻求美国批准的助推器剂量的双人特写镜头COVID-19疫苗。
该公司周三说,它已经开始申请程序的第三个剂量的疫苗都16岁以上。该公司表示,将与美国食品和药物管理局完成应用程序的这个星期。
FDA本月早些时候说,移植受者或其他较弱的免疫系统可以得到额外剂量的辉瑞或现代化疫苗。上周,美国卫生官员宣布给COVID-19加强注射所有美国人来支撑他们的保护在飙升三角洲冠状病毒的变体。
这一计划吸引了世界卫生组织的科学家的批评,他们指出,贫穷国家没有得到足够的疫苗初始轮的照片。
辉瑞疫苗,与德国BioNTech联合开发,获得完整的FDA批准本星期早些时候,也对于那些16岁以上。它已经给这个年龄段在紧急情况下使用授权,这仍然是那些年龄在12到15。
超过2亿剂量的辉瑞疫苗已经在美国——数百万更多的从12月开了绿灯。
在美国使用的三种疫苗由辉瑞公司现代化和强生仍从COVID-19预防住院和死亡。但疫苗不显得那么强烈反对高度传染性三角洲变体时对早期版本的病毒。
美国助推计划要求一个额外的剂量8个月后人们获取第二枪辉瑞或现代化的疫苗。
周三,强生表示收到了助推器单发疫苗的人看到大幅上涨抵抗病毒抗体。该公司计划向监管机构讨论其助推器。
现代化将会做同样的事情。周三说,它已经完成了应用程序FDA剂治疗疫苗的全部批准。
进一步探索
©2021美联社。保留所有权利。材料可能不会被出版,广播,重写或重新分配。