小说链接机制遗传缺陷在IBD患者肠道泄漏

生物医学科学家领导的研究小组在加州大学河滨分校,已经确定了一个新颖的机制丧失突变基因PTPN2,发现在许多炎症性肠病的患者,或炎症性肠病,影响肠道上皮细胞维持一个障碍。
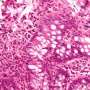
的肠上皮细胞,一个层细胞,发挥了至关重要的作用人类健康通过提供一个屏障,同时允许营养物质和水的吸收。肠上皮细胞需要调节免疫功能,与肠道菌群,防止肠道病原体infection-all极度依赖于一个完整的上皮屏障。
影响了约300万美国人,炎症性肠病是一组慢性肠道疾病,肠道内壁变得红肿和漏水的。增加肠道泄漏最近被证实患炎症性肠病的风险增加。
”这个新的出版物是一个高潮的身体在我的实验室工作鉴定丧失突变在PTPN2如何能增加肠道通透性或泄漏,”德克兰·McCole说,教授在加州大学医学院生物医学科学,领导这项研究发表的临床研究杂志。《华尔街日报》选择了研究论文作为一个“编辑突出。”
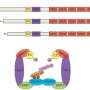
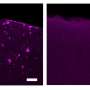
在这项研究中,这是在老鼠身上进行的,人类的细胞和组织的炎症性肠病病人,McCole和他的同事们发现,在IBD患者携带功能丧失PTPN2突变,claudin-2的表达,一种蛋白质,导致损失的水和钠进入肠道,促进腹泻,是增加。McCole实验室使用小鼠模型,确定了双重机制,解释了claudin-2表达增加,导致流体损失。
PTPN2通常作为制动claudin-2的表达,McCole解释道。PTPN2的功能丧失的突变发生在IBD删除这个刹车和允许流体损失增加。
”此外,PTPN2也促进内源性因素,称为matriptase,移除claudin-2从细胞膜的面积,它介导效应允许流体损失发生时,“McCole说。
减少PTPN2活动的累积效应在两个机制是提高流体损失。研究人员证明了这个缺陷可以通过治疗细胞缺乏PTPN2与recombinant-or synthetic-matriptase。
“我们工作改善的理解炎症性肠病的基因如何有助于改变生理驱动他们的症状的病人,“McCole说。“它还支持我们的相关工作识别多类的药物,称为激酶抑制剂,可用于救援的肠漏,尤其是在患者功能丧失突变在PTPN2基因。
研究还显示,最近发现和罕见的小说在PTPN2突变,导致肠道上皮损伤的孩子,也会增加肠道上皮leakiness-but不会引起上皮细胞死亡。
“这表明患者发展这种情况可能出现“肠漏”全面爆发的疾病发生之前,“McCole说。
的标题研究论文“t细胞蛋白质酪氨酸磷酸酶保护肠屏障功能通过限制上皮紧密连接重建。”
更多信息:罗纳德·r·Marchelletta et al T细胞蛋白质酪氨酸磷酸酶保护肠屏障功能通过限制上皮紧密连接重构,临床研究杂志(2021)。DOI: 10.1172 / JCI138230