PANoptosome:先天免疫反应的新边疆
圣裘德儿童研究医院免疫学家已经确定了免疫传感器是如何感染细胞组织和启动一个多方面的先天免疫反应与活病毒和细菌感染。发现出现在今天自然。
理解功能的研究提供一个新的范例和监管作用inflammasome传感器和细胞死亡复合物在感染。工作同样也强调了新的治疗靶点治疗的疾病,比如癌症和炎症性自身免疫性疾病与异常相关inflammasome传感器激活。
Inflammasomes蛋白复合物形成被感染细胞或细胞损伤。复合物包括传感器,识别不同的病毒,细菌和其他病原体或危险信号。Inflammasomes驱动炎症信号。这些信号激活炎症细胞死亡通路和消除感染但也可以有助于病理炎症。先前的研究都集中在inflammasomes独自工作。
“这新工作是建立在我们寻求识别inflammasome规定,“说通讯作者Thirumala-Devi Kanneganti,博士,圣裘德的免疫学。“我们的研究突显出inflammasomes和多个细胞死亡组件可以在大型——一起工作蛋白质复合体称为PANoptosome激活先天免疫反应和释放PANoptosis。”
Kanneganti实验室表明,监管和分子三个inflammasome传感器之间的交互,与细胞死亡的蛋白质,推动形成复杂的称为PANoptosome mega-cell死亡。而不是调节一种炎性细胞程序性死亡,PANoptosomes控制three-pyroptosis,细胞凋亡和necroptosis,称为PANoptosis。
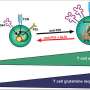
调查人员也确定AIM2 inflammasome传感器担任PANoptosome主监管机构组装在回应感染单纯疱疹病毒1和弗朗西斯氏菌属novicida细菌。AIM2也证明了感染帮助老鼠存活所必需的。
“发现解决核心问题领域的先天免疫,细胞死亡和inflammasome生物学,”Kanneganti说。
从inflammasomes PANoptosomes
Kanneganti的研究建立在之前的研究的实验室,这是一个领域的先驱。Kanneganti确定第一批inflammasome传感器和帮助建立inflammasome研究。
该领域的研究人员都集中在如何个人inflammasome传感器检测入侵的病原体或其他威胁。Inflammasomes历来被认为反应通过激活炎症细胞死亡途径之一。
Kanneganti实验室长期利益理解inflammasomes监管和已经确定细胞死亡通路之间的冗余。2016年,研究人员首次报道,流感感染活性分子在所有三个细胞死亡通路。科学家们称PANoptosis过程。调查人员还确定,一个先天免疫传感器称为ZBP1 flu-infected PANoptosis监管细胞。本研究为PANoptosis的发展奠定了基础研究领域。
PANoptosomes今天
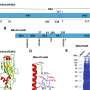
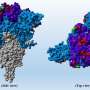
现在,Kanneganti集团认为AIM2主监管机构新的PANoptosome。第一作者SangJoon Lee博士,博士后Kanneganti实验室,用于免疫沉淀反应,显微镜和其他技术表明,AIM2其他inflammasome传感器Pyrin ZBP1,和细胞死亡的分子AIM2-PANoptosome的一部分。PANoptosome开车炎症细胞死亡。
“这是重要的证据表明inflammasome来自多个传感器和分子细胞死亡通路在同一个复杂和突出PANoptosome的角色在保护主人生活致病性感染,”李说。
病原体直播他们的存在更广泛的免疫系统,这有助于解释为什么感染引发PANoptosome组装和一种更健壮的免疫反应。病原体可以携带蛋白质,防止特定的细胞死亡通路的激活。PANoptosis保护宿主免疫系统提供了一个解决方案。
“我们的假设是,虽然工作传感器涉及可能会有所不同,大多数感染会诱发这些独特的先天免疫复合物的形成被称为PANoptosomes释放炎性细胞死亡,PANoptosis Kanneganti说。
进一步探索