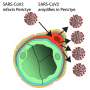
研究使用“模型”器官显示SARS-CoV-2感染广泛的细胞类型,甚至可以改变细胞的功能
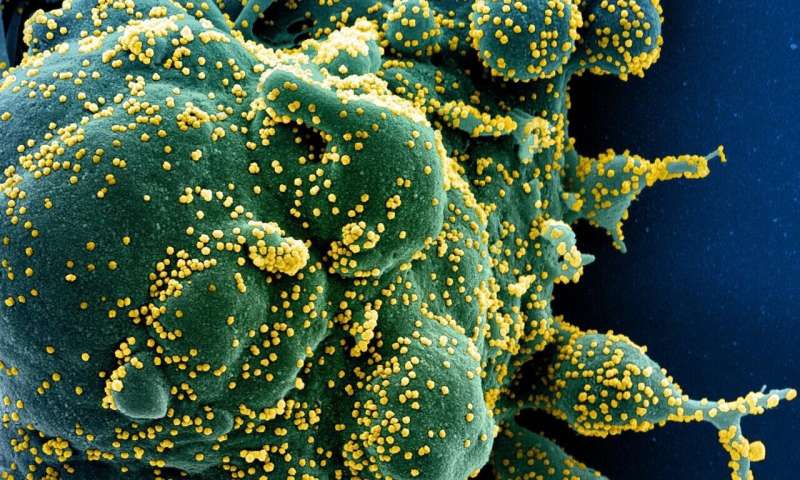
COVID-19的渗透能力和潜在变化的功能不同的细胞在体内,包括胰岛素的胰腺β细胞,是一次特别会议的主题在今年的欧洲研究协会的年会上糖尿病(2型)。Shuibing Chen博士表示将由外科学系,威尔康奈尔医学,纽约,纽约,美国
“COVID-19代表广泛的系统性问题引起的严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)。除了呼吸衰竭,许多个人与COVID-19存在多器官的临床并发症,包括心脏缺陷,胃肠道症状,肾脏损害、肝功能异常、神经症状和代谢异常,”Chen博士解释道。“因此,强烈需要开发一个方法来系统地研究SARS-CoV-2的影响感染在不同的宿主组织。”
本课程着重于人类多能干细胞(细胞可以发育成任何类型的细胞)和瀑样(集群类型的细胞在实验室条件下模拟特定器官的功能)系统地评估流程和在病毒感染细胞反应,屏幕也可能的药物以防止感染。
”筛选十个不同类型的细胞和瀑样,我们发现肺癌、结肠癌、心脏、肝脏、胰腺瀑样和多巴胺神经元可以被SARS-CoV-2感染,”陈博士说。“这项工作提出了第一个干细胞模型了解器官和细胞在这些器官可以被SARS-CoV-2感染,进而导致了临床试验研究COVID-19患者的β细胞功能。本研究工作仍在继续,”她解释说。
此外,Chen博士和她的同事报道第一organoid-based筛查研究,确定几个候选药物阻断SARS-CoV-2进入宿主细胞。
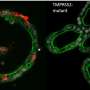
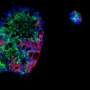
此外,他们进行单细胞RNA-sequencing和证实,多种类型的细胞在胰腺(胰岛细胞)容易SARS-CoV-2。在SARS-CoV-2感染,产生更少的菊粉和更多的α和β细胞显示腺泡的细胞标记。细胞仍然制造胰岛素,但感染意味着他们的胰岛素水平低得多。同时,受感染的β细胞也产生葡萄糖和消化酶,表明病毒有能力从根本上改变细胞命运(称为细胞分化转移)。
“这项研究表明SARS-CoV-2感染导致细胞命运变化的一个例子,它提供了进一步的洞察COVID-19的病理机制,”Chen博士解释道。她讨论了已有的案例报告新发糖尿病COVID-19感染后数周。“这是绝对值得调查的新发糖尿病患者在这个COVID-19大流行,”她说。
陈博士的研究小组还报道mini-heart组织模型显示造成的损害身体的巨噬细胞(免疫细胞)在心肌细胞攻击(心肌细胞)COVID-19患者。这项工作确定Janus激酶(激酶)抑制剂,保护心肌细胞从macrophage-mediated损害SARS-CoV-2感染。激酶抑制剂已经紧急使用授权COVID-19病人。当暴露于SARS-CoV-2,巨噬细胞分泌白细胞介素6和TNFalpha通过JAK / STAT通路损害心脏细胞。激酶抑制剂保护心脏细胞通过阻断这些通路的白细胞介素6和TNFalpha。
陈博士总结道:“瀑样可以作为一个强大的模型来研究病毒感染的潜力,宿主反应,免疫细胞介导宿主损伤和,最后,药物筛选。”
她的团队目前正在关注发展中多细胞瀑样模型和人性化的动物模型,它更精确地复制疾病患者个体的发展,并将这些模型应用于开发新的抗病毒药物。