轻推细胞修复受损的视网膜
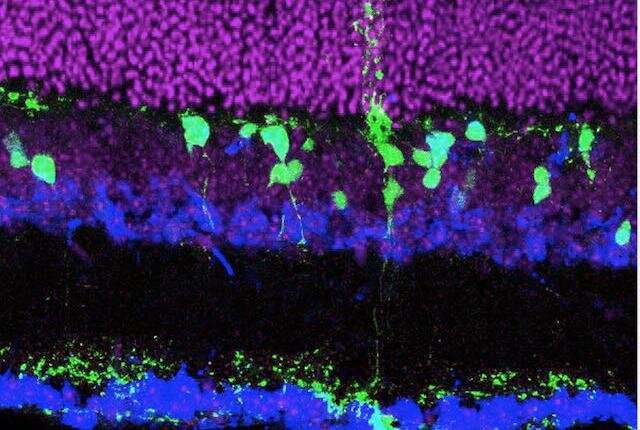
有一天可以使用一种方法来帮助修复因黄斑变性,青光眼和糖尿病等疾病而失去视力的患者的视网膜,西雅图华盛顿大学医学院的科学家诱导了非神经细胞。神经元。
“我们认为这项研究开辟了视网膜的基因疗法的可能性神经元失去了失踪。
描述方法和发现的论文出现在当今的问题中细胞报告。REH实验室的博士后研究员Levi Todd是该论文的主要作者。
在研究中,研究人员试图诱导细胞视网膜称为神经胶质细胞,产生神经元。多年来,视网膜和大脑中神经胶质细胞的主要工作被认为只是将神经元固定在适当的位置。Glia的名字在希腊语中表示“胶水”。现在已知神经胶质细胞是高度活性细胞,在神经元的培养和支持中起着至关重要的作用。
在某些物种(例如鱼类和纽约)中,神经胶质细胞可以通过区分各种神经元来修复受损的视网膜和脑组织。鸟类中的神经胶质细胞还具有有限的修复神经组织的能力。但是,在哺乳动物(例如大鼠,小鼠和人类)中,一旦它们成熟,神经胶质细胞就无法区分到其他细胞类型。因此,人的大脑和视网膜是大脑的延伸,无法修复自己。
在先前的研究中,REH及其同事发现,有可能诱导哺乳动物的神经胶质细胞退后一步,并成为一种更为不成熟的原始细胞类型,称为祖细胞。该状态的细胞具有沿许多发育途径向前发展并分化为多种细胞类型的灵活性。
为了诱导哺乳动物神经胶质细胞的这种变化,Reh和他的同事使用了称为的蛋白质转录因子。转录因子是与DNA结合并调节基因活性的蛋白质。反过来,这控制了确定细胞结构和功能的蛋白质的产生。
科学家首先确定了在鸟类视网膜中神经胶质细胞修复活性中似乎很重要的转录因子。然后,他们确定了小鼠中相应的转录因子。
在2017年发表的一项研究中,Reh和他的同事表明,一种称为Achaete-Scute家族BHLH转录因子1或ASCL1的转录因子可能会诱导小鼠视网膜神经胶质细胞成为祖细胞。这些细胞又可以区分视网膜神经元。
虽然表明有可能诱导神经胶质细胞产生神经元细胞是一个突破,但该方法效率低下。该方法仅诱导约30%的神经胶质细胞成为神经元,仅产生有限数量的不同类型的视网膜神经元。这些主要是一种称为双极细胞的中间神经元,视网膜细胞相互通信。
然而,在新的研究中,该团队仅添加一个称为Atonal BHLH转录因子或ATOH的另一个转录因子发现,可能会提示祖细胞开始沿着导致神经元细胞的发育途径开始。
正如他们在新论文中报道的那样,通过将ASCL1与ATOH的版本结合使用,称为ATOH1或ATOH7,科学家发现,不仅可以转换神经元细胞中的更多神经胶质细胞,而且可以产生更广泛的视网膜细胞类型也是如此。除了使用ASCL1生成的中间神经元外,ATOH1/7的添加现在启用了神经胶质再生神经节细胞,这些细胞在一种称为青光眼的眼部疾病中丢失。科学家还能够再生少量的光感应锥细胞,这些锥体是负责彩色视觉的,并且需要查看细节。
Reh说:“基本上,我们给细胞两个轻浮。”“第一次轻推神经胶质细胞退后一步,像祖细胞一样。下一个轻推驱动这些祖细胞状细胞向下移动到神经元细胞的路径。”
他补充说:“非常明显的是,新细胞自行组织自己并按照预期的方式连接,而不是原始单元,但它们似乎在做正确的事。它们也不完全成熟到成人细胞中但是,我们希望通过将它们暴露于其他化学信号中,它们会进一步成熟。”
研究结果表明,可以使用基因治疗技术将这些以及其他转录因子的遗传指示插入受损的视网膜中,并诱导视网膜修复自身。基因疗法已经被批准用于治疗称为RPE65突变相关视网膜营养不良的遗传性视力丧失原因。
Reh说:“开发针对更常见的视网膜疾病的基因疗法仍然是一条路,但是这些结果显示了这种恢复视力的前进的途径。”
博士后研究员Nik Jorstad和Marcus Hooper,Wes Jenkins,UW Molecular&Cellular Biology计划的研究生,计算机生物学家Connor Finkbebeiner,本科研究人员Alex Haugan,Nick Radulovich,Nick Radulovich,Claire Wong和Phoere Wong and Phoebe Donaldson,研究作为大学医学学院生理学与生物物理学教授弗雷德·里克(Fred Rieke),他的博士后研究员青陈(Qing Chen)。
进一步探索