欧盟默克制药机构看数据COVID-19药丸
欧盟药品机构周一开始回顾默克的COVID-19治疗药片,以便它可以迅速建议国家药品欧盟27国当局希望开始使用它之前,需得到官方认可。
欧洲药品机构在一份声明中表示,它将“欧盟建议在最短的时间内帮助国家当局决定可能的早期医学的使用,例如,在紧急情况下使用设置”。
总部位于阿姆斯特丹机构会给的建议而全面审查molnupiravir继续领先于市场的药物可能的应用。
目前大多数COVID-19治疗需要一个IV或注入。默克的COVID-19药丸已经由美国食品和药物管理局审查后表现出强烈的初步结果。周四,英国成为第一个国家好。
在英国,避孕药被批准为18岁以上成人COVID-19阳性和至少有一个风险因素发展严重疾病,如肥胖症或心脏病。患有轻度到中度COVID-19将四片药一天两次的五天。
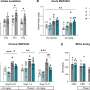
在美国,FDA已审查molnupiravir本月晚些时候公开会议。9月该公司公布其药物住院和死亡的利率下调50%。
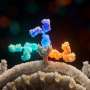
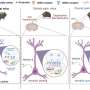
冠状病毒使用的药物靶标酶复制本身,插入到它的错误遗传密码缓慢,其传播和接管人类细胞的能力。基因活动使得一些独立专家质疑药物可能会引起突变导致出生缺陷或肿瘤。
©2021美联社。保留所有权利。材料可能不会被出版,广播,重写或重新分配。