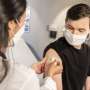
法国-奥地利公司Valneva的新冠疫苗正在接受欧盟审查

欧洲药品监管机构周四启动了对法国-奥地利生物技术公司Valneva生产的新冠病毒疫苗的加速审查,欧盟已经签署了一份多达6000万剂的协议。
欧洲药品管理局(EMA)表示,这种疫苗使用“灭活”病毒,而不是辉瑞或Moderna疫苗的新mRNA技术,在试验中显示它产生了对抗冠状病毒的抗体。
“EMA人类药物委员会已开始对新冠病毒——符拉拉2001 (VLA2001)进行滚动审查疫苗正在由瓦尔涅瓦开发,”这家总部位于阿姆斯特丹的监管机构在一份声明中表示。
它表示:“尽管EMA无法预测总体时间线,但由于滚动审查期间所做的工作,它对最终申请的评估时间应该比正常情况下要短。”
疫苗从审查阶段到批准通常需要几个月的时间,尽管俄罗斯和中国开发的疫苗等等待的时间更长。
11月10日,欧盟委员会宣布与瓦尔涅瓦公司达成协议,将在2022年和2023年分别提供约2700万剂和3300万剂疫苗。
该消息公布后,Valneva股价上涨,但并未完全抵消去年9月以来的跌幅。当时英国取消了1亿剂疫苗的订单,导致该公司市值蒸发逾一半。
这家总部位于南特斯的公司获得了法国政府的支持。在国家制药冠军赛诺菲和著名的巴斯德研究所遭遇挫折后,法国未能生产出COVID-19疫苗,令法国政府感到尴尬。
EMA表示,瓦尔内瓦的研究“表明,疫苗引发了针对SARS-CoV-2的抗体的产生,这是导致COVID-19的病毒,可能有助于预防这种疾病。”
它补充说:“EMA将在数据可用时对其进行评估,以决定收益是否大于风险。”
Valneva疫苗使用的灭活病毒方法与大多数流感疫苗和许多儿童疫苗相同卫生官员希望可以减少对一些新技术疫苗的怀疑。
到目前为止,EMA已经批准了四种用于欧盟成人的疫苗。
辉瑞-生物科技公司的美德疫苗和美国制药公司Moderna的疫苗使用了信使RNA技术。英国-瑞典阿斯利康-牛津疫苗和强生疫苗使用病毒载体技术。
美国制药公司诺瓦瓦克斯(Novavax)预计将在几周内做出申请批准的决定。
©2021法新社