体内自组装sirna治疗逆转亨廷顿舞蹈病
一项新的研究发表在大脑南京大学的陈曦教授和中山大学的钟培教授报道了体内自组装sirna治疗亨廷顿舞蹈病的逆转。
亨廷顿病是由亨廷顿(HTT)基因外显子1中的CAG重复扩增引起的,导致突变HTT (mHTT)蛋白的表达。mHTT蛋白聚集成细胞内包涵体,主要在皮层和纹状体诱导神经元死亡。虽然亨廷顿舞蹈症的基因起源已经被认识了20多年,但没有一种治疗方法可以治愈或减缓这种疾病的进程。
最近,基于寡核苷酸的治疗方法使用小干扰rna (siRNAs)和反义寡核苷酸(ASOs)已提供了有希望的治疗结果,减少毒性mHTT临床前研究但要实现寡核苷酸疗法在亨廷顿舞蹈病中的全部潜力,仍需克服一些主要挑战。
例如,寡核苷酸必须通过侵入性策略直接输送到大脑或脊髓液中;然而,寡核苷酸在纹状体的分布很差,纹状体是大脑深处的结构,是亨廷顿舞蹈病中受影响最严重的大脑结构。因此,需要一种方便、有效、安全的给药策略来改善寡核苷酸治疗药物的脑深部分布和神经元摄取。
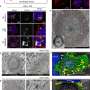
在这项研究中,联合研究小组设计了合成生物学电路来重新编程小鼠肝脏,以指导mHTT siRNAs的合成和自组装到分泌性外泌体中,并促进外泌体封闭的mHTT siRNAs到皮层和纹状体的传递。
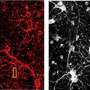
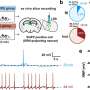
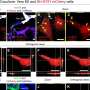
这一策略的治疗价值通过有效沉默mHTT蛋白和去除皮质和纹状体中的有毒聚集物得到证实,从而改善亨廷顿舞蹈病三种小鼠模型的行为缺陷和纹状体和皮质神经病理。总的来说,本研究建立了一种方便、有效和安全的sirna在体内自组装策略,可能为亨廷顿舞蹈病提供显著的治疗益处。
这些发现的科学意义如下:
(1)合成生物学回路以裸DNA质粒形成,通过静脉注射简单给药;然后,mHTT siRNA由肝细胞自发产生,并通过外泌体循环系统转移。这种设计借用了人体自身的小RNA组装和运输机制,避免了与传统递送技术相关的侵入性程序和安全问题,这可能为未来治疗亨廷顿病开辟新的途径。
(2)本研究为sirna向深海扩散奠定了基础大脑抑制有毒蛋白质聚集的区域。由于蛋白质聚集是许多神经退行性疾病的标志,体内自组装的sirna有望加速其他神经退行性疾病的治疗方法的发展,如帕金森病和阿尔茨海默病疾病.
(3)大多数合成生物学回路部署在微生物或永生细胞系中。本研究重新编程宿主肝脏执行用户定义的行为,允许在复杂的、动态的体内环境中精确控制siRNA分布和靶基因表达。这一创新策略超出了目前合成生物学在生物医学中的应用范式。
进一步探索