增强大脑辅助细胞中的一个基因可以减缓小鼠阿尔茨海默病的进展
在阿尔茨海默病小鼠模型中,增加辅助大脑神经元的细胞中一种基因的表达可以保护神经元。
这些发现来自于1月10日发表的一项新研究自然通讯.Nrf2基因的高活性可以减缓老年人认知能力和身体机能的衰退老鼠并减少了大脑中粘性蛋白质的积累,这些都是人类疾病的关键标志。
这项工作是由威斯康星大学麦迪逊分校药学院教授杰弗里·约翰逊和他在苏格兰爱丁堡大学的合作者领导的。
研究人员此前已经确定Nrf2是帕金森病和肌萎缩性侧索硬化症(ALS)的治疗靶点。他们现在正在寻找增加Nrf2活性的方法,作为阿尔茨海默病的潜在疗法,阿尔茨海默病几乎没有好的治疗方法,也没有治愈方法。
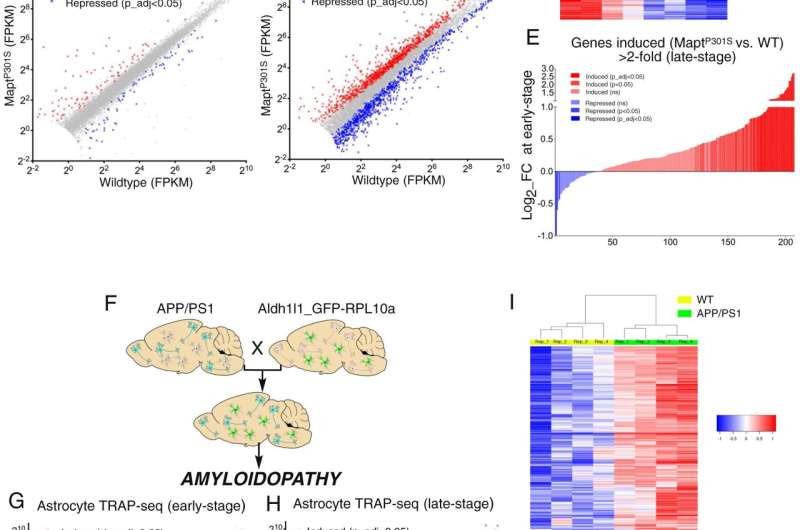
威斯康星大学麦迪逊分校领导的团队发现,在称为星形胶质细胞的支持细胞中增加Nrf2的水平,有助于神经元极大地减少阿尔茨海默氏症中心两种无序蛋白质的积累。
这些蛋白质,tau蛋白和β-淀粉样蛋白,形成危险的团块,分别称为缠结和斑块。这些蛋白质的积累会给神经元造成压力,破坏神经元的运作机制,导致神经元死亡和认知能力下降。
过度表达Nrf2的小鼠在记忆和物理测试中表现更好。在小鼠模型中,增强Nrf2还逆转了阿尔茨海默氏症的遗传特征,这表明它具有广泛的正常化作用,而不仅仅是解决tau和β -淀粉样蛋白的团块。
“β -淀粉样蛋白和tau蛋白的减少程度以及几乎完全逆转的遗传变化是非常重要的,”约翰逊说,在这项研究之前,他帮助确定了Nrf2在其他神经退行性疾病中通过星形胶质细胞的保护作用。“超过2300基因阿尔茨海默氏症模型中大脑的一个部分发生了变化。几乎所有2300人都恢复了正常。我惊呆了。我从没想过我们会得到这样的结果。”
Nrf2控制着许多基因的表达,这些基因可以防止氧化应激或炎症等损害。它在老年痴呆症晚期被激活,但它的激活可能为时已晚,无法保护大脑免受疾病的侵害。
为了研究在星形胶质细胞中持续激活Nrf2是如何保护大脑的,约翰逊的实验室培育了小鼠,它们在神经元周围过度积累β -淀粉样蛋白,以模拟阿尔茨海默病,并在星形胶质细胞中大量表达Nrf2。
与没有Nrf2基因增强的小鼠相比,那些拥有大量Nrf2基因的小鼠大脑中的β -淀粉样蛋白减少了近90%。他们的β -淀粉样斑块也少得多。
无论是老鼠还是人类,阿尔茨海默氏症的症状之一就是记忆丧失。在经典的记忆测试中,过度表达Nrf2的阿尔茨海默氏症模型小鼠也比没有这种增强基因的小鼠表现得更好——几乎和非阿尔茨海默氏症小鼠一样好。而且,拥有额外Nrf2基因的小鼠在通过类似绳索的杆时表现得更好,这是一种衡量它们平衡和协调能力的指标。
爱丁堡大学的合作者贾尔斯·哈丁厄姆和他的团队对积累了过多tau蛋白的小鼠进行了类似的实验。他们发现,当星形胶质细胞Nrf2也增加时,tau含量高的小鼠保留的神经元多了25%。这些小鼠在大脑皮层神经元中积累的tau蛋白也更少。
“Nrf2过表达在tau蛋白和β -淀粉样蛋白模型中都有非常相似的影响,”哈丁厄姆说。“在这两种情况下,很明显,星形胶质细胞中的Nrf2正在调节神经病理。”
研究小组怀疑Nrf2增强了神经元消化这些蛋白质的能力,从而将它们清除出去。基因是如何不被表达的神经元但在附近的支持性星形胶质细胞中,这一壮举仍不清楚。此外,Nrf2似乎提供了额外的好处这些还没有被很好地理解,比如在很大程度上逆转大脑中与疾病相关的基因变化。
虽然Nrf2是抗阿尔茨海默病治疗的一个有吸引力的候选者,但它已被证明很难在大脑中被激活大脑过去吸毒。约翰逊说,新一代的治疗方法,如治疗性肽和基因疗法,可能是激活基因的更好方法。
开发阿尔茨海默病有效治疗方法的另一个关键因素是更早地诊断患者。研究人员发现,阿尔茨海默氏症需要很多年,甚至几十年才能完全发展。尽早治疗可能会改善患者的预后。
“目前正在开发的新诊断工具将非常有用,”约翰逊说。
进一步探索