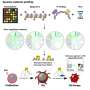
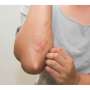
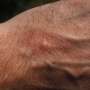
FDA批准Rinvoq用于治疗特应性皮炎
制造商周五宣布,美国食品和药物管理局批准Rinvoq (upadacitinib)用于治疗12岁及以上患者的中重度特应性皮炎。
批准是为了病人与特应性皮炎,没有反应以前治疗并不能很好地控制与其他药物或当使用其他药物不建议。12岁及以上、体重至少40公斤(88磅)的患者可开始使用15mg Rinvoq;年龄小于65岁的患者在此剂量下未达到足够的反应,剂量可增加至30mg,每日一次。
批准是基于三项研究中2500多名患者的疗效和安全性数据。这些患者中约52%曾接受过系统性特应性皮炎治疗。在16周的三项研究中,患者接受每日一次的Rinvoq(15毫克和30毫克)单药治疗和联合治疗外用糖皮质激素达到了湿疹面积和严重程度指数至少减少75%的主要终点,以及特应性皮炎的有效研究者总体评估为透明或几乎透明(0/1),与基线相比至少减少了两个等级。与安慰剂相比,早在Rinvoq治疗的第一周,就可以看到最严重瘙痒数值评定量表≥4的显著改善。
Rinvoq在特应性皮炎患者中的安全性与类风湿关节炎患者相似。其他不良反应专门针对患有特应性皮炎包括疱疹性湿疹/卡波西氏静脉曲张疹。Rinvoq的严重副作用包括结核病等感染,50岁及以上至少有一种心血管风险因素的人群死亡风险更高,某些癌症风险增加,以及血栓。
艾伯维获得批准。
更多信息:更多信息请访问在这里。
2022每日健康。版权所有。