鉴定出血液系统恶性肿瘤的新治疗靶点
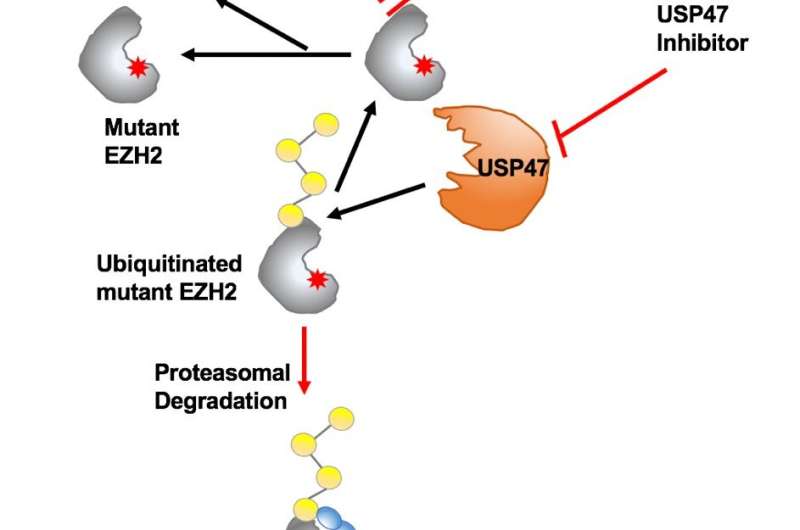
据中国科学院的赫菲物理学研究所的科学家称,抑制泛素特异性肽酶47(USP47)被确定为具有突变蛋白EZH2的血液系统恶性肿瘤的新型治疗靶点。结果发表在白血病。
该研究的第一作者Yang Jie表示,这是一种有选择地稳定突变体EZH2的去泛素化酶(DUB)。
血液学恶性肿瘤是从产生血液的骨髓开始的癌症。最近,Zeste同源物2(EZH2)的表观遗传调节剂增强剂已成为弥漫性大B细胞淋巴瘤(DLBCL)和成人急性骨髓性白血病(AML)的关键靶标,其高频突变。然而,二次突变和酶活性无关EZH2引起耐药性长期治疗酶抑制剂。因此,破坏突变的EZH2蛋白可能在靶向EZH2突变体癌和耐药性过高的情况下更有效。
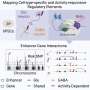
在这项研究中,使用化学遗传筛查并与临床前模型研究结合使用,杨和她的同事发现,小分子化合物诱导了泛素介导的突变体EZH2的降解,从而导致AML和DLBCL细胞死亡的体外和体内。
通过广泛的选择性分析,他们发现USP47是一种新型的配音稳定突变体EZH2,也是突变体EZH2阳性血液学恶性肿瘤的潜在治疗靶标。
从机械上讲,USP47在表达EZH2突变的细胞中高度表达,与WT EZH2相关并稳定突变体EZH2。在正常细胞中抑制USP47备件WT EZH2,从而规避临床治疗中的不良副作用。
他们确定了USP10在AML中选择性靶向FLT3-ITD和激酶抑制剂耐药剂FLT3突变体,而在AML中选择性靶向JAK2-V617F的JOSD1抑制剂。
“突变体EZH2的治疗靶向通过DUB促进其降解抑制而不是抑制其酶活性是一种创新的方法,可以帮助克服对当前EZH2酶抑制剂的抵抗。”杨说。
“我们的发现提供了潜在的好处不良副作用与EZH2抑制相关的临床抑制以及克服与EZH2激酶抑制相关的技术限制,以降低临床疗效。
进一步探索