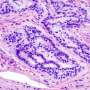
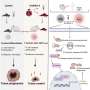
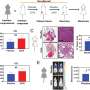
研究人员恢复了一种基因的功能,该基因可以抑制肝癌并增强免疫治疗
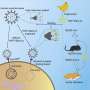
来自麻省总医院(MGH)和布莱根妇女医院(BWH)的一组研究人员通过使用mRNA纳米颗粒重新编程了肝癌的肿瘤微环境。这项技术类似于新冠病毒疫苗中使用的技术,恢复了大脑的功能p53控制调节基因,一种肿瘤抑制基因不仅在肝脏中发生突变,而且在其他类型的癌症中也发生突变。当与免疫检查点阻断(ICB)联合使用时,p53 mRNA纳米颗粒方法不仅诱导了肿瘤生长的抑制,而且还显著增加了肝细胞癌(HCC)实验室模型的抗肿瘤免疫反应。研究结果发表在自然通讯.
BWH纳米医学中心的共同资深作者Jinjun Shi博士说:“肿瘤微环境的细胞和分子成分的重编程可能是治疗HCC和其他癌症的一种革命性方法。”他与MGH肝癌生物学家和共同资深作者Dan G. Duda博士共同开发了这个平台。“通过使用这种新方法,我们瞄准了特定的通路肿瘤细胞信使rna纳米颗粒。这些微小的颗粒为细胞提供了构建蛋白质的指令,在HCC的情况下,这延缓了肿瘤的生长,并使肿瘤对免疫疗法的治疗更敏感。”
HCC是最常见的肝癌形式,其特点是死亡率高,患者预后差。免疫检查点阻滞剂是一种革命性的新型药物,可使人体免疫系统识别和攻击癌细胞,已在治疗HCC中显示出疗效,但大多数患者并未受益。为了克服这种耐药性,人们正在开发多种策略,通过将icb与其他现有疗法(如抗vegf药物和放疗)相结合来改善icb。然而,即使这些方法也只能使少数患者受益,因此迫切需要新的联合疗法。
受到mRNA在COVID-19疫苗中成功应用的鼓舞,Shi决定将该技术(经过一定的修改)应用于靶向癌细胞。他与Duda合作,后者的MGH实验室已经创建了复杂的动物模型,以分析肝脏肿瘤的微环境对免疫治疗的反应。他们开发并优化了一种信使rna纳米颗粒策略,以恢复失去的功能p53这是一种肿瘤抑制基因,其功能在超过三分之一的HCC病例中丧失。在此过程中,他们发现了p53通过调节癌细胞与免疫细胞的相互作用来调节肿瘤微环境的证据,这是ICB治疗的一部分。
“在我们之前的工作中,我们开发了靶向cxcr4的纳米颗粒,这是一种由肝脏表达的趋化因子受体癌症并选择性地共同传递激酶抑制剂等药物,”Duda解释说。“我们现在已经适应了这个平台,使用CXCR4作为一种邮政编码,用纳米颗粒包裹治疗性mrna选择性地靶向肿瘤。当我们将这种纳米药物与抗程序性死亡受体1 (PD-1)抗体(HCC患者的一种标准免疫疗法)结合使用时,它诱导了肿瘤微环境的全局重编程肿瘤通过恢复响应p53表达。”
研究小组的下一步是将他们的研究从动物模型转移到临床试验中的患者身上。几十年来,科学家们一直在努力寻找一种有效的方法来针对这种疾病肿瘤抑制基因Shi强调道。“我们的概念验证研究是一项令人兴奋的进展,它清楚地表明p53 mRNA纳米颗粒与ICB联合使用不仅有效,而且可以通过逆转HCC和其他潜在癌症的免疫抑制而产生重大影响。”
Shi是哈佛医学院(HMS)的麻醉学副教授。Duda是HMS放射肿瘤学副教授,MGH GI放射肿瘤学转化研究主任。肖玉玲博士和陈江医学博士是这项研究的主要作者和HMS的博士后研究员。
进一步探索