胎盘可能为早期自闭症的诊断和干预提供线索
加州大学戴维斯分校精神研究所的一项新研究发现,一种新的人类基因与胎儿大脑发育和自闭症谱系障碍(ASD)有关。这一发现还将该基因与母亲产前早期的维生素使用和胎盘氧水平联系起来。
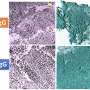
《科学》杂志2月16日发表的一项研究表明基因组生物学在美国,研究人员利用基因组测序技术发现了一种DNA甲基化特征胎盘新生儿最终被诊断为自闭症。这个标志与胎儿早期神经发育有关。
该研究的主要作者、加州大学戴维斯分校微生物学和免疫学教授珍妮·拉萨尔(Janine LaSalle)说:“通过采用公正的方法研究胎盘DNA甲基化差异,我们在与自闭症相关的基因组中一个定位不佳的区域发现了一个新基因。”
自闭症谱系障碍是一种复杂的神经系统疾病,与遗传和环境因素.美国疾病控制与预防中心(CDC)估计,每44名儿童中就有1名被诊断为自闭症谱系障碍。男性比女性更普遍。
为什么研究胎盘很重要
胎盘支持子宫内胎儿的发育。它调节氧气供应和新陈代谢,并提供对胎儿大脑发育至关重要的激素和神经递质。
“胎盘是一个经常被误解和忽视的组织,尽管它在调节和反映子宫内大脑发育的关键事件方面很重要。它就像一个时间胶囊,用来发现子宫里发生的事情。LaSalle说:“几十年来,尽管胎盘组织是寻找儿童结局分子线索的金矿,但医院分娩时却把胎盘扔掉了。”
在怀孕期间,胎儿可能会经历氧化应激自由基和抗氧化剂在体内的失衡。这在正常的大脑发育中很常见。然而,在某些情况下,暴露于空气污染和杀虫剂等环境因素会导致过度氧化应激。这种状态会导致细胞和组织损伤或神经发育迟缓。
“氧化应激是正常的。但过度的氧化应激可能来自与ASD相关的环境暴露,如空气污染、农药、母亲肥胖和炎症,”LaSalle说。
表观基因组是一组化合物和蛋白质,它们告诉DNA该做什么。这些化合物附着在DNA上并改变其功能。其中一种化合物是CH3(被称为甲基),从而导致DNA甲基化。新生儿表观基因组可以反映早期发育过程中遗传和环境因素之间的相互作用。它还可能影响未来的健康结果。
胎盘是一个很有前途的组织,可以用来鉴定在胎儿大脑中也起作用的基因的DNA甲基化变化。本研究探讨了ASD与胎盘DNA甲基化的关系。
在母亲胎盘中寻找可能预测自闭症的因素
研究人员研究了204名儿童的发育情况,这些儿童的母亲都参加了MARBLES和EARLI的研究。这些母亲至少有一个较大的孩子患有自闭症,并且被认为有更高的可能性有另一个孩子患有自闭症。当这些孩子出生时,母亲的胎盘被保存下来以供将来分析。
在36个月时,孩子们接受了诊断和发展评估。基于这些测试,研究人员将这些儿童分为“典型发育”(TD)、“患有ASD”和“非典型发育”(Non-TD)。
研究人员还从胎盘组织中提取并量化了DNA。他们将胎盘样本分为发现组、复制组和特异性复制组。
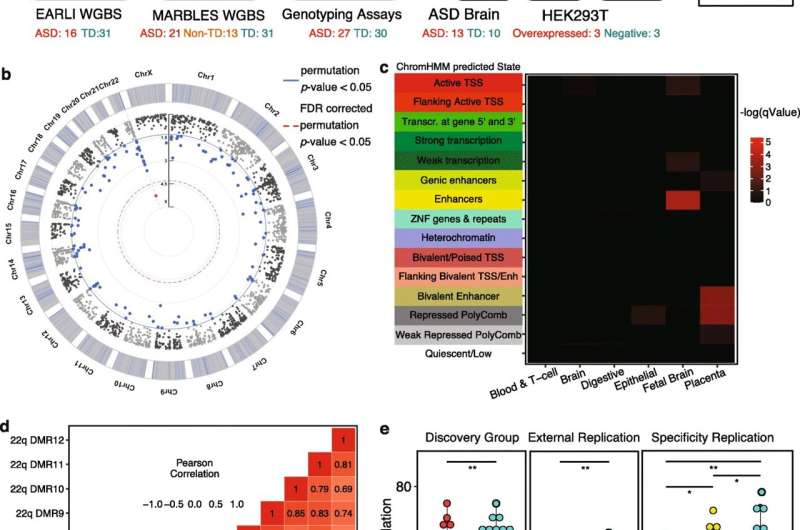
研究小组使用全基因组亚硫酸盐测序(WGBS)和全基因组测序(WGS)对来自MARBLES研究的92个样本(46个ASD, 46个TD)进行了分离和测序。为了确定差异甲基化在不同人群中是否可重复,复制组包括来自EARLI研究的16个ASD和31个TD样本的WGBS数据。
特异性复制组来自MARBLES研究的21个ASD, 13个Non-TD和31个TD胎盘样本。研究人员使用这些样本来确定甲基化变化是否是自闭症特有的。
最后,他们对41名ASD儿童和37名TD儿童进行了全基因组测序。
胎盘揭示与ASD相关的基因
研究人员在22号染色体上的22q13.33位点发现了ASD中差异甲基化的一个区域,这个区域以前与ASD没有联系。他们在该区域定位并鉴定了一个名为LOC105373085的新基因,并将其重新命名为NHIP(神经元缺氧诱导,胎盘相关)。
为了了解该基因的功能,他们检测了人类细胞系和脑组织中NHIP的表达水平。他们测试了NHIP对缺氧的反应,即组织中低氧水平的状态。研究人员发现,NHIP是一种在缺氧后神经元中被激活的基因,并调节其他与神经元发育和氧化应激反应有关的基因通路。较高的NHIP水平增加了胚胎细胞系的细胞分裂。
这一点很重要,因为在胎盘中,缺氧会引发胎盘细胞分裂,进一步与母体血管接触,为发育中的大脑提供足够的氧气。
研究人员还发现,与TD样本相比,NHIP在ASD胎盘和大脑中的激活程度较低,这支持了NHIP在预防ASD方面的保护作用。
LaSalle说:“我们发现NHIP基因在大脑中很活跃,对氧化应激有反应,并影响与自闭症相关的其他已知基因的表达。”“在大多数怀孕中,胎盘会经历一些不可避免的压力。我们认为NHIP是为了缓冲过度氧化应激的影响。”
产前维生素和自闭症
这项研究的另一个显著发现是产前维生素在调节NHIP的工作中所起的作用。产前维生素富含叶酸,可以减少氧化应激。
在22q13.33 NHIP区域具有遗传差异的个体中,怀孕第一个月服用产前维生素显示出显著的保护作用。在怀孕的第一个月服用产前维生素似乎提供了必要的代谢元素,以抵消NHIP对氧化应激反应性降低的基因遗传。
LaSalle说:“与之前的研究一致,我们发现在计划怀孕时服用产前维生素是必不可少的。”“我们的研究结果提供了关键的见解,可能有助于识别更容易患自闭症的新生儿,让他们更早地进行干预,或者只是知道要早点观察他们。”
研究人员指出,在用于诊断之前,这些结果还需要进一步的复制。
更多信息:朱一辉等,胎盘甲基组揭示与自闭症相关的22q13.33脑调控基因位点,基因组生物学(2022)。DOI: 10.1186 / s13059 - 022 - 02613 - 1